Генетические ограничения эффективности и безопасности массовых вакцинаций населения
Аннотация. Низкая эффективность массовой иммунизации населения и поствакцинальные осложнения не всегда связаны с неудовлетворительным качеством вакцин или нарушением техники вакцинации, допущенных медицинским персоналом. В работе показано, что динамика эпидемического процесса, наиболее характерная для него клиническая картина болезни, эффективность и безопасность вакцинации, частота поствакцинальных осложнений среди прочих факторов находятся в тесной зависимости от относительного количества в популяции лиц с дефектами (полиморфизмами) генов иммунной системы и физиологических систем, препятствующих развитию болезни. Полиморфизация таких генов происходит спонтанно, путем образования снипов и делеций, распределяющихся в следующих поколениях в соответствии с законами Менделя. Накоплению полиморфизмов, участвующих в патогенезе инфекционной болезни, как это не парадоксально, способствовал достигнутый прогресс в борьбе с контагиозными циклическими инфекциями и, в частности, с натуральной оспой. Было снято селективное давление на популяции людей, устранявшее индивидуумов с дефектами иммунной и других систем организма, не способных эффективно отвечать на инвазию возбудителя инфекционной болезни. Темпы накопления полиморфизмов возрастают в относительно генетически однородных популяциях (жители островных государств), и в популяциях, практикующих браки между родственниками. Отказаться от борьбы с возбудителями контагиозных циклических инфекций невозможно. Поэтому необходимо ожидать дальнейшего роста регистрируемых случаев поствакцинальных осложнений, причины которых следует искать в геноме вакцинированного человека и, соответственно, внести коррекции в стратегию массовой иммунизации различных групп населения и методологию выяснения причин поствакцинальных осложнений. В работе также описаны полиморфизмы аллелей генов иммунной системы, достоверно ассоциирующиеся с низкой эффективностью вакцинации против кори, краснухи, эпидемического паротита, гриппа, гепатита В и осложнениями, возникающими после вакцинации живой противооспенной вакциной и туберкулезной вакциной на основе Mycobacterium bovis BCG.
Библиографическое описание: Супотницкий МВ. Генетические ограничения эффективности и безопасности массовых вакцинаций населения Актуальная инфектология 2015; (1): 100–15.
Summary. Low efficiency of cohort immunization and postvaccinal complication are not always connected with vaccine unsatisfactory quality or violation of vaccination requirements by medical workers. The paper demonstrates that epidemic dynamics, disease clinical manifestation typical for it, efficiency and safety of immunization, postvaccinal complications incidence also closely interrelate with relative quantity of persons with anomalies (polymorphism) of immune response genes and physiologic systems protected from disease development. Polymorphism of these genes has a spontaneous development by single nucleotide polymorphism and deletions forming apportioning in next generations according to Mendel's laws. Polymorphism accumulation involved into infectious diseases pathogenesis is ironically a result of progress in control of contagious cycle infections, particularly natural smallpox. There was taken off a selective pressure from a population that extracted persons unable to react effectively on infectious agents invasion. Velocity of polymorphism accumulation is growing in relatively genetically homogeneous population (inhabitants of island countries) and in populations with typical intermarriages. It is impossible to refuse from control of contagious infectious agents. So we should expect of increase of registered postvaccinal complication associated rather with human genome peculiarity than with other reasons. That causes the necessity to adjust a strategy of immunization of various cohorts and methods for determining the reasons of postvaccinal complications. The paper also describes polymorphism of immune response genes significantly associated with low effectiveness of vaccination against measles, rubella, epidemic parotitis, B hepatitis and complications after live smallpox and tuberculosis vaccine Mycobacterium bovis BCG.
Bibliographical description: Supotnitskiy МV. Genetic-associated reduced efficiency and safety of cohort immunization. Actual Infectology 2015; (1): 100–15.
Резюме. Низька ефективність масової імунізації населення і поствакцинальні ускладнення не завжди пов'язані з незадовільною якістю вакцин або порушенням техніки вакцинації, що допустив медичний персонал. У роботі показано, що динаміка епідемічного процесу, найбільш характерна для нього клінічна картина хвороби, ефективність і безпека вакцинації, частота післявакцинальних ускладнень серед інших факторів перебувають у тісній залежності від відносної кількості в популяції осіб з дефектами (поліморфізм) генів імунної системи і фізіологічних систем, перешкоджають розвитку хвороби. Поліморфізація таких генів відбувається спонтанно, шляхом утворення сніпів і делецій, що розподіляються в наступних поколіннях відповідно до законів Менделя. Накопиченню поліморфізмів, що беруть участь у патогенезі інфекційної хвороби, як це не парадоксально, сприяв досягнутий прогрес у боротьбі з контагіозними циклічними інфекціями, і зокрема з натуральною віспою. Було знято селективний тиск на популяції людей, що усуває індивідуумів з дефектами імунної та інших систем організму, не здатних ефективно відповідати на інвазію збудника інфекційної хвороби. Темпи накопичення поліморфізмів зростають у відносно генетично однорідних популяціях (мешканці острівних держав) і в популяціях, що практикують шлюби між родичами. Відмовитися від боротьби зі збудниками контагіозних циклічних інфекцій неможливо. Тому необхідно очікувати подальшого зростання реєстрованих випадків поствакцинальних ускладнень, причини яких слід шукати в геномі вакцинованої людини і, відповідно, внести корекції в стратегію масової імунізації різних груп населення і методологію з'ясування причин поствакцинальних ускладнень. У роботі також описані поліморфізми алелей генів імунної системи, що вірогідно асоціюються з низькою ефективністю вакцинації проти кору, краснухи, епідемічного паротиту, грипу, гепатиту В та ускладненнями, які виникають після вакцинації живою противіспенною вакциною і туберкульозною вакциною на основі Mycobacterium bovis BCG.
Библиографическое описание: Супотницький МВ. Генетичні обмеження ефективності та безпеки масових вакцинацій населення. Актуальна iнфектологiя 2015; 1: 100–15.
В руководствах по иммунопрофилактике инфекционных болезней низкая эффективность вакцинации и поствакцинальные осложнения обычно объясняются нарушениями «холодовой цепи» при транспортировке и хранении вакцин или небрежностью, допущенной медицинским персоналом уже при проведении вакцинации [1]. Однако далеко не всегда эти нарушения удается доказать. Кроме того, у разных людей ответы иммунной системы на вакцинацию одной и той же вакциной различаются по максимальному уровню специфических антител в сыворотке крови, авидности антител, продолжительности их циркуляции в кровеносном русле, продолжительности иммунологической памяти, цитокиновым ответам и другим параметрам [2]. Следовательно, проблемы эффективности и безопасности вакцинации населения выходят за пределы контроля показателей качества вакцин, утвержденных соответствующими нормативными документами; и правильности проведения самой вакцинации. Они неизбежно упираются в особенности генетической организации иммунной системы и других систем организма человека, участвующих в патогенезе болезни. Цель настоящей работы – показать генетические ограничения эффективности и безопасности массовых вакцинаций населения.
В работе мы рассмотрим причины накопления в популяциях людей мутаций в генах, чья экспрессия связана с эффективным ответом иммунной и других систем организма на вторжение возбудителя инфекционной болезни, обобщим сведения о таких генах и проанализируем роль этих мутаций как в клиническом течении инфекционной болезни, так в развитии поствакцинального процесса.
Устойчивость и восприимчивость к возбудителям инфекционных болезней. Относятся к полигенным пороговым наследственным признакам. Люди, наследственно восприимчивые к возбудителю инфекционной болезни, не заболевают, если не было их экспонирования к этому возбудителю. Люди устойчивые к этому же возбудителю, заболевают при превышении определенного порога дозы заражения. Вне эпидемического процесса такие признаки могут рассматриваться как нейтральные. Селективными они становятся при контакте с возбудителем инфекционной болезни, и их носители подпадают под действие естественного отбора. Частота встречаемости отдельных генов (аллелей генов) в инфицированной популяции людей варьируют. Поэтому наблюдается множество переходных вариантов патологии между типичными формами проявления инфекционной болезни[1] (рис. 1).
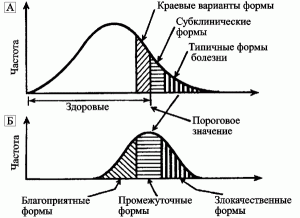 Рис. 1. Клинические признаки инфекционной болезни при полигенной устойчивости и восприимчивости к патогенному микроорганизму. А. Разнообразие стертых и субклинических вариантов инфекционной болезни, которые образуют непрерывный переход от нормы до выраженных форм ее типичного проявления. Б. Множество переходных вариантов патологии между типичными формами проявления инфекционной болезни [3].
Рис. 1. Клинические признаки инфекционной болезни при полигенной устойчивости и восприимчивости к патогенному микроорганизму. А. Разнообразие стертых и субклинических вариантов инфекционной болезни, которые образуют непрерывный переход от нормы до выраженных форм ее типичного проявления. Б. Множество переходных вариантов патологии между типичными формами проявления инфекционной болезни [3].
За более чем 200 лет, прошедших с начала массовых вакцинаций против натуральной оспы по способу, предложенному Эдвардом Дженнером (Edward Anthony Jenner, 1749–1823), популяционный состав населения изменился. Натуральная оспа, доминировавшая среди эпидемических болезней на протяжении столетий, исчезла, и ее селективное давление на популяции людей, прекратилось. В отличие от чумы, вспыхивавшей опустошительными эпидемиями с временными промежутками в несколько десятилетий, и, даже, столетий, натуральная оспа присутствовала среди людей постоянно. Годовые колебания смертности различались в разы, но не на порядки. С 1667 г. по 1800 г. число умерших от натуральной оспы в Лондоне на 1000 умерших от других причин составляло в среднем 65 человек в год. Но это была иная оспа по охватываемому ею контингенту, по сравнению с тем, что врачи наблюдали в ХХ в. До практики массовых вакцинаций натуральная оспа представляла собой исключительно детскую болезнь, которой болели все дети до года. Европейские врачи еще в начале XVIII в. придерживались точки зрения авторов раннего средневековья Рази и Авиценны, что оспа является врожденной болезнью. Она развивается у ребенка в результате брожения менструальной крови матери, которой тот питался, находясь в ее утробе. Такое понимание причин возникновения натуральной оспы держалось несколько тысяч лет [5].
Губерт [5] привел данные шведских и британских статистических исследований XVII–XVIII вв., свидетельствующие о том, что летальность среди детей, заболевших натуральной оспой, была постоянной на протяжении нескольких столетий, и не превышала 6–10 % от количества заболевших. Только в начале XVIII в., когда натуральная оспа по неизвестным причинам стала менее распространенной болезнью и появилось большое количество людей, не перенесших ее в детстве, врачи пришли к выводу о ее заразности.
Современные данные о механизмах иммунного ответа у человека на ВНО говорят о том, что в первую очередь от натуральной оспы погибают индивидуумы, иммунная система которых не способна эффективно отвечать на инвазию вируса выработкой нейтрализующих антител. У таких пациентов оспа развивается в геморрагической форме, вирус в высоких титрах обнаруживается в фарингеальном тракте, увеличивая риск передачи болезни «по цепочке» [6][2]. То есть натуральная оспа на протяжении столетий изымала из популяций индивидуумы, имеющие генетические дефекты иммунной системы. Свой «вклад» в селекцию генотипов вносили другие контагиозные болезни — грипп, корь и др. (рис. 2).
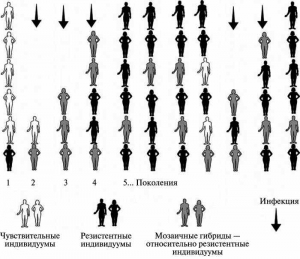 Рис. 2. Формирование возбудителями контагиозных инфекций популяционной резистентности к инфекционным болезням. За основу взята схема Rumyantsev [7].
Рис. 2. Формирование возбудителями контагиозных инфекций популяционной резистентности к инфекционным болезням. За основу взята схема Rumyantsev [7].
Poland et al. [8] относят к генетическим дефектам иммунной системы полиморфизмы генов главного комплекса гистосовместимости (МНС); цитокинов; рецепторов цитокинов; мембранных рецепторов, узнаваемых вирусами (membrane-based viral receptors); толл-подобных рецепторов; рецепторов витаминов А и D; сигнальных молекул и др. Полиморфизмы генов, продукты которых вовлечены в ответы иммунной системы, находятся в сложной ассоциации с полиморфизмами генов, обуславливающими популяционные особенности населения на территории, где происходит распространение инфекционной болезни. Примеры таких ассоциаций приведены в табл. 1.
Таблица 1
Примеры популяционной ассоциации клинических форм микобактериальных инфекций с полиморфизмами генов, участвующих в иммунных ответах*
|
Инфекционная болезнь |
Ассоциация клинических форм болезни с отдельными аллелями генов людей |
Популяция |
|
Лепра |
МНСII-DR (лепроматозная и туберкулоидная) |
Индийцы, бразильцы |
|
TNFα (лепроматозная) |
Индийцы |
|
|
NRAMP1 (лепра per se) |
Вьетнамцы |
|
|
VDR (лепроматозная и туберкулоидная) |
Индийцы |
|
|
Туберкулез |
МНС II-DR2 (легочный туберкулез) |
Индийцы |
|
МНС II-DRB1 (легочный туберкулез) |
Индийцы |
|
|
МНС II-DQB1 (быстрое прогрессирование туберкулеза) |
Камбоджийцы |
|
|
МНС II-DQB1 (легочный туберкулез) |
Индийцы |
|
|
NRAMP1 (легочный туберкулез) |
Гамбийцы, канадские индейцы |
|
|
VDR (легочный туберкулез) |
Гамбийцы |
|
|
MBL (легочный туберкулез, туберкулезный менингит) |
Индийцы, цветные |
|
|
IL-1Rα/IL-1β (туберкулоидная форма) |
Гуджаратцы |
|
|
Атипичные микобактериальные инфекции |
IFNγR1 |
Мальтийцы, тунисцы, итальянцы, немцы, португальцы |
|
IFNγR2 |
Англичане |
|
|
IL-12RB1 |
Марокканцы |
|
|
IL-12p40 |
Пакистанцы |
* По [9]
Ошибочно считать, что устойчивость человека к заражению возбудителем инфекционной болезни и способность его организма противодействовать развивающимся патологическим процессам, зависят только от ответов его иммунной системы. A.L. Rasmussen et al. [10] показали связь выраженности экспрессии генов рецепторов эндотелиальной тирозинкиназы (endothelial receptor tyrosine kinase) Tie1 и Tek (Tie2) с клиническим течением лихорадки Эбола. В экспериментах на генетически модифицированных мышах они обнаружили, что коагулопатия при лихорадке Эбола наиболее выражена у тех линий животных, у которых экспрессия Tie1 и Tek подавлена.Экспрессия этих генов активирует коагулирующие факторы системы крови, такие как тромбин (F2), тканевой фактор (tissue factor, F3), и рецепторы, активируемые протеазами (protease activated receptors 1, 3 и 4; PAR1/F2R, PAR3/F2RL2, PAR4/F2RL3), что снижает риск развития тромбогеморрагического синдрома. По их мнению, полиморфизмы генов Tie1 и Tek могут определять клиническое течение и летальность при лихорадке Эбола у людей в природных очагах этой болезни. Однако влияние генетических дефектных физиологических систем организма человека на патогенез инфекционной болезни, изучено гораздо хуже, чем роль в этих процессах различных генетических дефектов иммунной системы.
Главный комплекс гистосовместимости (major histocompatibility complex; MHC, ГКГС)[3]. Это группа антигенов клеточной поверхности, играющих важную роль в клеточном узнавании и в ответах иммунной системы, направленных на подавление инфекционного процесса. Молекулы I класса МНС связывают и презентируют пептиды микроорганизма CD8+T-лимфоцитам; молекулы II класса МНС связывают и презентируют пептиды микроорганизма CD4+T-лимфоцитам, что обеспечивает координацию действий различных звеньев иммунной системы в подавлении инфекционного процесса. Щель, связывающая пептиды микроорганизма (peptide-binding clefts), образованная молекулами МНС, содержит высокополиморфные кластеры аминокислот, способные ограничивать спектр пептидов, презентируемых T-лимфоцитам. В тех случаях, когда белки МНС не в состоянии связать пептидный фрагмент чужого антигена, Т-хелперы остаются ареактивными и их помощь В-клеткам не реализуется.
Белки МНС кодируются большим семейством генов со сложной интрон-экзонной организацией. Наследуются кодоминантно. У человека гены МНС находятся в хромосоме 6 (6p21). Общее число фенотипов МНС составляет около 20 млрд. Сиквиенс-анализ генов 8 различных гомозиготных МНС-гаплотипов[4] позволил выявить у них до 44 тыс. однонуклеотидных полиморфизмов (single nucleotide polymorphism, SNP; произносится как снип) и вставок/делеций, а также подтвердить наличие более чем 300 локусов, включающих более 160 белок-кодирующих генов (protein-coding genes). И те и другие в кодирующих или регуляторных регионах генов МНС приводят к изменениям в структуре и функции экспрессируемых белков. Средняя плотность снипов для генов МНС варьирует от 1 до более чем 60 на т.п.о. ДНК[5]. Наиболее полиморфными являются гены, относящиеся к молекулам I и II классов МНС (рис. 3).
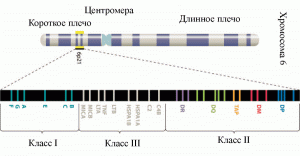 Рис. 3. Схематическое расположение на хромосоме 6p21 генов, кодирующих белки МНС классов I и II. В пределах генов MHC также находятся гены факторов комплемента C2 и C4B; фактора некроза опухолей (ген TNF); лимфотоксина-α (ген LTA); белка теплового шока А (ген HSPA), высоковариабельных цепей MHC класса I (гены MICA и MICB) — их условно относят к генам MHC класса III (другое название — non-HLA genes). Более подробно см. http://www.nature.com/nrg/journal/v5/n12/poster/MHCmap/poster.pdf. По J.M. Blackwell et al. [11].
Рис. 3. Схематическое расположение на хромосоме 6p21 генов, кодирующих белки МНС классов I и II. В пределах генов MHC также находятся гены факторов комплемента C2 и C4B; фактора некроза опухолей (ген TNF); лимфотоксина-α (ген LTA); белка теплового шока А (ген HSPA), высоковариабельных цепей MHC класса I (гены MICA и MICB) — их условно относят к генам MHC класса III (другое название — non-HLA genes). Более подробно см. http://www.nature.com/nrg/journal/v5/n12/poster/MHCmap/poster.pdf. По J.M. Blackwell et al. [11].
Молекулы I класса МНС (HLA-A, -B, -C, -E, -F, и -G) экспрессируются на поверхности всех ядросодержащих клеток, формирующих ткани, и представляют собой гетеродимеры, включающие тяжелую α-цепь и однодоменный β2-микроглобулин, нековалентно связанный с основным полипептидом. Связывание антигенного пептида молекулой I класса происходит в антигенсвязывающей щели, образованной α-спиральными участками α- и α2-доменов. Антигены I класса определяют индивидуальную антигенную специфичность. При вирусной инфекции они вызывают гибель инфицированных вирусом фагоцитирующих клеток [12].
Молекулы II класса МНС (HLA-DR, -DQ, -DM, и -DP) — гетеродимеры, состоящие из двух нековалентносвязанных цепей: α и Р, каждая из которых включает два домена (α1α2 и β1β2, соответственно). МНС класса II обеспечивают взаимодействие между макрофагами и В-лимфоцитами. Они участвуют в формировании всех видов иммунного ответа: противомикробного, трансплантационного, противоопухолевого и др. Связь между свойствами МНС и классами генов представлена в табл. 2.
Таблица 2
Связь между свойствами МНС и классами генов*
|
Свойства |
Гены класса I |
Гены класса II |
|
Интенсивное отторжение трансплантанта |
++++ |
+ |
|
Образование антител |
++++ |
++++ |
|
Стимуляция бласттрансформации |
+ |
++++ |
|
Реакция «трансплантант против хозяина» |
+ |
++++ |
|
Клеточная реакция аллогенного лимфолиза |
++++ |
|
|
Контроль силы иммунного ответа |
+ |
++++ |
|
Уровень рестрикции |
Лизис клеток-мишеней |
Антигенпредставляющая клетка |
|
Распределение антигенов по тканям |
Повсеместно |
Преимущественно макрофаги и В-лимфоциты |
*По [13]
Среди европейского населения наиболее часто отмечены гаплотипы, включающие антигены МНС-A3 и МНС-B7; МНС-А2 и МНС-В7; МНС-A1 и МНС-B8; МНС-A2 и МНС-B15; МНС-A2 и МНС-B35 и другие. Среди лиц монголоидных популяций частоты антигенов МНСA-A9 и 11 за счет снижения МНС-A1. Среди африканцев наблюдался подъем концентрации антигена МНС-A30 за счет снижения частоты встречаемости антигенов МНС-A1, 2 и 11[6]. Частоты встречаемости отдельных антигенов МНС среди этнических групп и населения, проживающего на различных территориях, не только отличаются, но и меняются со временем, но рассмотрение этих процессов не входит в задачу данной работы[7]. В табл. 3 показана частота встречаемости антигенов МНС среди 600 здоровых доноров крови Москвы
Таблица 3
Частота встречаемости антигенов МНС среди 600 здоровых доноров крови Москвы*
|
Наименование антигена |
Частота встречаемости антигенов (%) |
Наименование антигена |
Частота встречаемости антигенов (%) |
|
МНС-A2 |
50,8 |
МНС-Cwl |
10,0 |
|
МНС-Cw4 |
27,0 |
МНС-Cw6 |
10,0 |
|
МНС-A1 |
26,1 |
МНС-A26 |
9,3 |
|
МНС-B7 |
25,0 |
МНС-B13 |
8,8 |
|
МНС-A3 |
24,1 |
МНС-B18 |
8,5 |
|
МНС-A9 |
23,3 |
МНС-B14 |
8,3 |
|
МНС-Cw3 |
19,0 |
МНС-B17 |
7,8 |
|
МНС-35 |
18,0 |
МНС-27 |
7,0 |
|
МНС-B8 |
16,0 |
МНС-BI6 |
5,7 |
|
МНС-Cw2 |
16,0 |
МНС-A28 |
5,1 |
|
МНС-B5 |
14,0 |
МНС-A30 |
4,5 |
|
МНС-B12 |
13,3 |
МНС-A32 |
4,5 |
|
МНС-B15 |
13,0 |
МНС-B21 |
4,5 |
|
МНС-40 |
13,0 |
МНС-A31 |
3,0 |
|
МНС-A25 |
12,3 |
МНС-22 |
3,0 |
|
МНС-Cw5 |
11,0 |
МНС-A29 |
1,6 |
|
МНС-11 |
10,3 |
|
|
* По Кутьиной и с соавт. (1984). Взято с сайта http://2146777.ru/articles.php?id=31
Ассоциация полиморфизмов генов МНС с тяжестью течения инфекционного процесса. С полиморфизмом генов МНС связано такое явление, как не эффективный контроль иммунного ответа (см. табл. 1). Иммунная система людей с таким генетическим дефектом не реагирует на некоторые критические эпитопы патогенов, и инфекционная болезнь у них развивается значительно легче, ее клиническое течение проходит тяжелее, чем у тех лиц, у которых Т-хелперы активируются. Поэтому при анализе распределения аллелей МНС в популяции, люди с аллелью, неспособной к связыванию данного антигена, обнаруживаются среди больных в статистически значимых ассоциациях.
Другая причина ассоциации полиморфизмов МНС с отдельными инфекционными болезнями заключается в том, что антигенные структуры возбудителя инфекции имитируют или моделируют молекулы МНС. Развивается аутоиммунитет в отношении молекул МНС, и дисфункция и истощение Т-клеток. Иммунная система утрачивает способность противодействовать возбудителю инфекционной болезни (рис. 4).
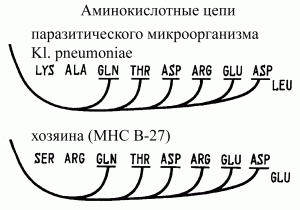 Рис. 4. Схема антигенной мимикрии между Klebsiella pneumoniae и МНС человека. Гомологичный участок Kl. pneumoniae и антигены гистосовместимости человека (МНС B-27) имеют 6 из 9 пар сходных аминокислот. По [15].
Рис. 4. Схема антигенной мимикрии между Klebsiella pneumoniae и МНС человека. Гомологичный участок Kl. pneumoniae и антигены гистосовместимости человека (МНС B-27) имеют 6 из 9 пар сходных аминокислот. По [15].
Учитывая то, что МНС играет универсальную роль в реакциях распознавания и взаимодействия на клеточном уровне, то можно предположить существование намного большего количества генетически опосредованных механизмов влияния комплекса на сопротивляемость организма к инфекционным болезням. В табл. 4 перечислены ассоциации, установленные между различными полиморфизмами МНС и некоторыми инфекционными болезнями. Указаны лишь антигены, обнаруживаемые в статистически значимой ассоциации.
Таблица 4
Связь между полиморфизмами МНС и некоторыми инфекционными болезнями*
|
Болезнь |
Связь с МНС |
|
Бактериальные |
|
|
Анкилозирующий спондилоартрит |
В27 |
|
Болезнь Рейтера |
В27 |
|
Острый передний увеит |
В7 |
|
Микобактериальные |
|
|
Туберкулез и лепра |
DR2 |
|
(мультибациллярные формы) |
(DRB1*1501, 1502) |
|
Лепроматозная форма лепры |
DR2 и DQ1 |
|
Туберкулоидная форма лепры |
DR3 |
|
Вирусные |
|
|
Лихорадка Денге |
DR15 |
|
СПИД (ВИЧ 1) |
DR13, DRB1*1301, 1302, 1303), DR2, (DRB1*1501), DRB1*03011 |
|
Гепатит В |
DR13 |
|
Гепатит С |
А2, DR5 |
|
Вирус Эпштейна—Барра |
В35.01 А11 В7 |
|
Паразитарные |
|
|
Малярия |
В53 |
|
Чесотка |
А11 |
|
Диффузный кожный лейшманиоз |
А11, В5, В7 |
|
Локализованный кожный лейшманиоз |
A28, Bw22, DQw8, Bw22, DR11, Qw7, Bw22, Dqw3 |
|
Шистосомоз |
B5, DR3 |
|
Висцеральный лейшманиоз |
А26 |
*По [16].
С одними и теми же полиморфизмами МНС в отдельных этнических группах ассоциируют сразу несколько инфекционных болезней, например, ВИЧ, возбудители гепатита В, проказы и туберкулеза среди представителей этносов негроидной расы в Африке.
Ку-лихорадка (Q-fever). Клиническая картина при Ку-лихорадке отличается разнообразием. У пациентов, носителей аллели DRB1*11, перенесших Ку-лихорадку, наблюдается осложнение, названное «слабостью после Ку-лихорадки» (post-Q-fever fatigue patients, QFS). У макрофагов людей, носителей данной аллели, обнаружена пониженная секреция интерферона-гама и IL-2 в ответ на стимуляцию лигандами в короткоживущих культурах [17].
Малярия. Установлена связь между аллелью B53 и защитой от тяжелых форм малярии — церебральной и сопровождающейся развитием выраженной анемии [18]. Аллель DRB1 ассоциирована с резистентностью к развитию анемии во время болезни [19].
Хантавирус Puumala. Индивидуумы, экспрессирующие гены аллели B8, переносят болезнь более тяжело. У них хантавирусная инфекция проявляется пониженным артериальным давлением, повышенным содержанием креатинина в крови. Одновременно наблюдается большее количество вируса в моче и крови. У лиц с аллелью B27 болезнь протекает в мягкой форме. Почти все больные с гаплотипом A1-B8-DR3, у которых прогрессивно развивался шок, одновременно экспрессировали аллель TNF2. Аллель связана с повышенной продукцией фактора некроза опухолей макрофагами в ответ на инфекцию [20].
Болезнь Лайма. Показана связь аллели DRB1*0401 с развитием хронических артритов после перенесения болезни Лайма и отсутствием со стороны организма человека реакции на антибиотикотерапию. Эта аллель связана также с повышенным риском развития тяжелых ревматоидных артритов. При исследовании антительных ответов у пациентов, перенесших болезнь Лайма, реакции иммуноглобулина G (IgG) на поверхностный наружный белок A (OspA) и OspB спирохеты часто обнаруживались в самом начале длительно текущих артритов. После проведения курса лечения антибиотиками у пациентов с аллелью DR4 и антительными ответами на OspA и OspB, артриты продолжались значительно дольше, чем в тех случаях, когда ответы на данные белки отсутствовали [21].
Лепра. В разных этнических группах предрасположенность к лепре и клиническое течение болезни проявляются по-разному благодаря полиморфизму МНС. Наличие аллели DR2 определяет предрасположенность человека к обеим формам проказы (туберкулоидной и лепроматозной). Среди некоторых народов Индии и Бразилии аллель ассоциирована с лепроматозной формой проказы. Среди египтян — с туберкулоидной формой. DQ-аллели, особенно DQw1, ассоциированы с туберкулоидной лепрой среди населения Индии, Кореи, Таиланда и Японии и с лепроматозной формой болезни среди отдельных групп населения Индии и Японии. DQ-аллели встречаются вместе с аллелью DR2. Аллель DR3 ассоциирована с туберкулоидной формой проказы среди населения Мехико, Суринама и Венесуэлы. Для отдельных аллелей MHC класса I также установлена связь с развитием разных клинических форм лепры, но пока наблюдения одних исследователей не находят подтверждения в работах других [22].
Туберкулез. Выявлена связь между легочной формой туберкулеза и полиморфизмами MHC. Аллели DR2 и DR3 ассоциируются с легочным туберкулезом и туберкулоидной проказой. DR2 определяет восприимчивость больного к легочному туберкулезу, и резистентность к антитуберкулезным препаратам [22,23].
Клещевой энцефалит. Среди больных клещевым энцефалитом в Хабаровском крае обнаружено статистически достоверное увеличение частоты встречаемости антигена MHC А3 (р<0,001). Реже, чем в популяции, встречались такие антигены как MHC А11, А19, А28, В35 (р<0,01) и Cw3 (р<0,001). Установлено учащение встречаемости в популяции антигена А3 (р<0,001) при стертой форме болезни; А3, В15, В16, В27 (р<0,001) — при менингеальной форме болезни; А3, А10, В16, Cw7 (р<0,001) — при очаговых формах клещевого энцефалита [24].
Ниже рассмотрим проявления полиморфизмов генов МНС в ответе на иммунизацию различными вакцинами.
Иммунопрофилактика кори, свинки и краснухи[8]. Специфические аллели генов белков классов I и II МНС ассоциированы с вариациями уровня антител в сыворотке после однократной вакцинации MMR-вакциной (measles-mumps-rubella vaccine) [25,26,27]. В частности аллели генов, относящихся к классу II DRB1*03, DQA1*0201 и классу I B8, B13 и B44, ассоциированы с низким уровнем противокоревых антител у вакцинированных здоровых американских школьников. В случае МНС-гомозиготности вакцинированных пациентов, показано значительное снижение уровня специфических антител после однократной вакцинации либо даже их отсутствие. Повторная вакцинация коревой вакциной, увеличение ее дозы при однократной вакцинации, позволяли преодолеть генетическую рестрикцию иммунного ответа [28]. Также установлено, что гаплотипы DRB1*07–DQB1*02–DPB1*02 и DRB1*07–DQB1*03–DPB1*04 находятся в строгой ассоциации с низким уровнем антител в ответ на вакцинацию коревой вакциной. Для гаплотипа A*26–Cw*12-B*38 показана строгая ассоциация с высоким уровнем антител и пролиферации лимфоцитов в ответ на вакцинацию против вируса эпидемического паротита [29]. Супертипы (supertype) B44 и B58 строго ассоциированы с низким уровнем противокоревых антител. Наиболее часто встречающийся супертип B7 ассоциирован с высоким уровнем специфических антител.
При оценке результатов вакцинации против эпидемического паротита (свинка) установлена ассоциация аллели МНС-DQB1*0303 с низким титром специфических антител [30]. Аллели МНС-A (*2402 и *6801) ассоциированы с низким содержанием в сыворотке крови IFN-γ (показатель выраженности клеточного иммунитета), который должен вырабатываться в ответ на вакцинацию живой вакциной против краснухи [31]. Таким образом, ответы на введение MMR-вакцины со стороны обоих звеньев иммунитета, клеточного (лимфопролиферация и секреция цитокинов) и гуморального (антитела), зависят от полиморфизмов МНС-генов [32].
Иммунопрофилактика гриппа. Основной ответ со стороны иммунной системы человека направлен на трансмембранные гликопротеины вируса гриппа: гемагглютинин (hemagglutinin, H) и нейраминидазу (neuraminidase, N). Производные эти же гликопротеинов составляют основу коммерческих гриппозных вакцин. Показана ассоциация МНС A*1101 (p=0,0001) и A*6801 (p=0,09) аллелей с высокими титрами антител к H1- и H3-гемагглютинининам у здоровых субъектов, вакцинированных тривалентной гриппозной вакциной, содержащей вирусные антигены штаммов вируса гриппа A/H1N1 New Caledonia/20/99, A/H3N2 California/7/2004 и B/Shanghai/361/2002 [33,34]. Однако у индивидуумов с аллелью МНС DQB1*0603–9/14 антител в ответ на вакцинацию не образовывалось [35].
Иммунопрофилактика натуральной оспы. При однократной вакцинации живой оспенной вакциной Dryvax™, высокие уровни противооспенных антител ассоциировались с аллелями класса II DQB1*0302 (p=0,003) и DQB1*0604 (p=0,03)[9]. Еще более четкая корреляция с выраженными иммунными ответами на вакцинацию была установлена для аллелей генов, кодирующих белки МНС класса I: МНС-B*1501 (p=0,006), B*3508 (p=0,02), B*4901 (p=0,04), B*5701 (p=0,04), B*5802 (p=0,05), C*0303 (p=0,01) и C*0704 (p=0,02). С низкими уровнями в сыворотке крови IFN-γ ассоциировались гены, кодирующие белки МНС класса I: B*3701 (p=0,03), B*4001 (p=0,03), B*5301 (p=0,04), B*5601 (p=0,03), C*0102 (p=0,03), C*0702 (p=0,04) и C*0801 (p=0,01) [36].
Иммунопрофилактика гепатита В. Вакцинация оказывалась неудачной у индивидуумов с аллелями DRB1*03, DRB1*07 и DQB1*03. Антитела либо не образовывались, либо их обнаруживали в сыворотке крови в низком титре [37,38,39]. Thursz [40] считает, что эти данные также свидетельствуют о возможности большей чувствительности этих пациентов к инфицированию вирусом гепатита В и длительном поддержании инфекции в персистентном состоянии.
Полиморфизмы генов цитокинов и их рецепторов. Эффективность иммунного ответа на антигены вакцин и способность иммунной системы формировать длительную иммунную память, находятся в зависимости от обмена сигналами между клетками иммунной системы, осуществляемого с помощью низкомолекулярных белков — цитокинов. Их продуцентами являются лимфоциты, макрофаги, гранулоциты, ретикулярные фибробласты, эндотелиальные клетки и другие типы клеток.
TNFα (tumor necrosis factor, фактор некроза опухоли) — цитокин, активирующий макрофаги и способствующий презентации антигенов посредством MHC класса II. Является важным модулятором продукции хемокинов, необходимых для эффективной миграции лейкоцитов в очаг воспаления. Низкая продукция TNFα недостаточна для активизации макрофагов до того уровня, когда они способны затормозить инфекционный процесс. Избыточная продукция TNFα вызывает расстройства гемодинамики (снижает сократимость миокарда, минутный объем крови, диффузно увеличивает проницаемость капилляров), цитотоксический эффект на клетки организма.
Наибольшее значение в эпидемиологии проявления тяжелого клинического течения инфекционной болезни имеет аллель TNF*2, ассоциированная с повышенным синтезом макрофагами фактора некроза опухолей. TNF*2 отличается от распространенной аллели TNF1 более сильным транскрипционным активатором, способствующим увеличению экспрессии TNFα. Повышенная продукция TNFα усиливает прогрессирование инфекционной болезни через локальные повреждения тканей, и повышает вирулентность патогенов. Установлено, что повышенное в сравнении с нормой количество TNFα в альвеолярных макрофагах людей усиливает рост M. tuberculosis [41]. Чрезмерная продукция TNFα ассоциируется также со слизисто-кожным лейшманиазом [42], рубцовой трахомой [43], церебральной малярией [44]и фатальными исходами при менингококковых заболеваниях [45]. Эта же аллель способствует более тяжелому течению инфекции, вызываемой хантавирусом Puumala [46].
Лимфотоксин α (lymphotoxin α, LTA; ранее назывался TNFβ). Ген LTA локализован на хромосоме 6p21 в непосредственной близости к гену TNFα и кодирует лимфотоксин — хемокин, секретируемый лимфоцитами и натуральными киллерными клетками. Растворимый α-лимфотоксин представляет собой гомотримеры (homotrimers), способные связываться теми же рецепторами, что и TNFα. В тоже время гетеродимеры (heterotrimers) формируют связанный с мембраной β-лимфотоксин, взаимодействующий с рецепторами β-лимфотоксина. Через эти рецепторы лимфотоксины вызывают плейотропные (pleiotropic) иммуномодуляторные эффекты. Локус MHC класса II, включающий LTA, был связан с чувствительностью бразильцев к лепре. Также с повышенной восприимчивостью к лепре у бразильцев ассоциирован гаплотип TNF*1/LTA*2, но не TNF*1/LTA*1. Эти данные предполагают причастность варианта гена лимфотоксина α — LTA*2 к развитию эпидемий проказы в отдельных популяциях населения Бразилии [47].
Снипы — самая распространенная причина полиморфизма генов цитокинов и их рецепторов и, соответственно, различий в уровне цитокиновой секреции клетками иммунной системы в ответ на антигенный раздражитель. Обнаружена ассоциация между наличием снипов в структурных и регуляторных участках генов TNFα, IL6 (ген интерлейкина 6) и IL1R (ген антагониста рецептора к интерлейкину 1В) и слабыми гуморальным иммунным ответом на однократное введение коревой вакцины [48,49]. Эти же исследователи по результатам двукратной вакцинации паротитной вакциной установили строгую ассоциацию снипов в генах IL12RB2 и IL12RB1 с дозозависимым снижением титров антител и клеточными ответами, соответственно [30]. Ими показано, что наличие снипов в генах IL10 (интерлейкин 10) и IL12RB2 (рецептор интерлейкина 12) ассоциировано со слабыми гуморальными и клеточными ответами на введение коревой вакцины. В тоже время, наличие снипов в гене IL2 (интерлейкин 2) ассоциировано с выраженными гуморальными и клеточными ответами на коревую вакцину [49].
Полиморфизмы цитокиновых генов могут проявляться поствакцинальными осложнениями. Stanley et al. [50], исследуя причины развития лихорадки (t≥37,7°C) у пациентов, вакцинированных оспенной вакциной DryvaxTM, обнаружили, что лихорадочная реакция на введение вакцины находится в достоверной ассоциации со специфическими гаплотипами IL1-генного комплекса на хромосоме 2 и гаплотипом в пределах гена IL18 на хромосоме 11. Обнаружена связь миоперикардита, возникающего у человека после вакцинации DryvaxTM, с отдельными гаплотипами IL1, IL18 и др. Полиморфизмы генов IL1, IL4 или IL18 являются причиной таких же поствакцинальных осложнений у пациентов после иммунизации MMR-вакциной и др. [51,52].
Недостаточная экспрессия IL-12 и его клеточного рецептора (IL-12Rβ1) приводят к снижению секреции IFN-γ NK- и T-клетками и, соответственно, к недостаточности клеточно-опосредованного иммунного ответа. Крупная делеция в гене IL-12, наследуемая по аутосомально-рецессивному типу, ассоциирована с диссеминацией туберкулезной вакцины на основе штамма BCG у детей [53]. Аналогичные наблюдения сделаны H.Elloumi-Zghal et al. [54] при исследовании детей с генерализацией вакцины BCG (лихорадка, аденопатия разной локализации, гепатоспленомегалия и др.). Ими показана гетерогенность мутаций в гене рецептора IL-12 (IL-12Rβ1) и зависимость клинического течения болезни от типа мутации. Однако у родителей этих детей мутаций в гене IL-12Rβ1 обнаружено не было. Авторы объясняют накопление таких мутаций среди жителей Туниса распространением в этой стране близкородственных браков.
Тяжелое клиническое течение генерализация вакцины BCG приобретает у новорожденных детей с мутацией в гене рецептора IL-2 (IL-2Rγ), что связано с ключевой ролью IL-2 в индукции пролиферации В-лимфоцитов и цитотоксических Т-лимфоцитов, и синтезе и секреции других лимфокинов: IL-4, IL-6, γ-интерферона, колоний-стимулирующих факторов (CSFs), факторов некроза опухолей (TNFs) [55].
Интерфероны. Под интерферонами понимают группу сходных по свойствам белков-цитокинов, подавляющих внутриклеточное размножение вирусов. Интерферон-α и интерферон-β продуцируются лейкоцитами и фибробластами; γ-интерферон — продукт CD4 Т-клеток воспаления, CD8 Т-клеток, натуральных киллеров. Врожденная недостаточность системы интерферона снижает способность фагоцитирующих клеток противодействовать размножению бактериальных возбудителей инфекционных болезней. Вспышки болезней, вызванные малопатогенными микобактериями Mycobacterium fortuitum, M. chelonei, M. avium, M. smegmatis, бациллы Кальмета-Герена (M. bovis) и др., являются следствием присутствия в человеческих популяциях какого-то порогового количества людей с мутациями в следующих четырех генах: IFN-γR1 (рецептор γ-интерферона 1), IFN-γR2 (рецептор γ-интерферона 2), IL-12Rβ1 (рецептор β1 интерлейкина-12) и IL-12p40 [19,56].
Ген IFN-γR1 расположен в регионе хромосомы 6q22q23. Различные мутации гена приводят к разным последствиям. Например, если ген IFN-γR1 полностью утратит способность к экспрессии белков, формирующих рецептор, то на поверхности клетки такого рецептора не будет. Известны так же мутации, приводящие к экспрессии на клеточной поверхности мутантных белков, способных связывать IFN-γR1, однако не трансдуцирующих сигнал по сигнальным путям клетки [57].
Мутантный ген IFN-γR1 обычно обнаруживают у родственников в семьях больных туберкулезом. В зависимости от типа наследования (рецессивного и доминантного) и этнической принадлежности человека, носителя мутации, меняется клиника осложнения и уменьшаются шансы на возможность эффективной терапии. У представителей французского этноса мутация гена IFN-γR1 приводит к диссеминации BCG и летальному лептоменингиту [58]; у японцев — к тяжелым формам BCG-остеомиелита [59], что, возможно связано с относительной генетической однородностью японского этноса, изолированно проживающего на островах уже более тысячи лет. Полная инактивация гена IFN-γR1 приводит к развитию летальной лепроматоидной BCG-инфекции [58]. На рис. 5 на примере трех семей показан процесс накопления в популяции людей с мутациями гена IFN-γR1.
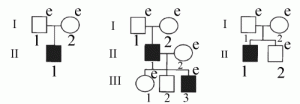 Рис. 5. Процесс накопления в популяции людей с мутациями гена IFN-γR1 на примере родословных трех японских семей. Поколения обозначены римскими цифрами, индивидуумы — арабскими цифрами. Пациенты с доминирующей частичной недостаточностью IFN-γR1, страдающие тяжелым BCG-остеомиелитом или подверженностью к микобактериальным инфекциям, показаны черными квадратами. e (examined) — проведено генетическое исследование на наличие мутации в гене IFN-γR1. Только у одного родственника обнаружено аутосомно-доминантное наследование мутации, у остальных они возникали спонтанно. По [59].
Рис. 5. Процесс накопления в популяции людей с мутациями гена IFN-γR1 на примере родословных трех японских семей. Поколения обозначены римскими цифрами, индивидуумы — арабскими цифрами. Пациенты с доминирующей частичной недостаточностью IFN-γR1, страдающие тяжелым BCG-остеомиелитом или подверженностью к микобактериальным инфекциям, показаны черными квадратами. e (examined) — проведено генетическое исследование на наличие мутации в гене IFN-γR1. Только у одного родственника обнаружено аутосомно-доминантное наследование мутации, у остальных они возникали спонтанно. По [59].
Внешне процесс накопления в популяции людей с мутациями гена IFN-γR1 будет проявляться учащением случаев осложнений, возникающих у детей после вакцинации вакциной BCG, что ошибочно можно принять за результат плохого контроля качества вакцины производителями. Процесс накопления мутаций в гене IFN-γR1 далеко не случаен, так ген располагается в участке хромосомы, участвующем в ее репликации, где высока вероятность возникновения спонтанных мутаций вследствие ошибок в спаривании нуклеотидов[10] [57].
В двух независимых клинических исследованиях обнаружена ассоциация двух несинонимичных снипов в гене метилентерахлоридфолатредуктазы (methylenetetrahydrofolate reductase gene)[11] и двух снипов в гене фактора регуляции интерферона (IFN regulatory factor-1 gene),[12] с тяжелыми осложнениями (лихорадка, лимфоаденопатия или генерализованная сыпь), развивающимися после вакцинации живой оспенной вакциной APSV (Aventis Pasteur smallpox vaccine) [60].
Клеточные рецепторы, не относящиеся к цитокиновым. Такое деление рецепторов, участвующих в иммунных ответах на патогенные микроорганизмы, условно. В данной работе оно проведено для отделения иммунных реакций, управление которыми осуществляется низкомолекулярными белками — цитокинами, от тех которые вызываются непосредственным взаимодействием патогенного микроорганизма с рецепторами клеток.
Толл-подобные рецепторы — класс клеточных рецепторов с одним трансмембранным фрагментом, распознающие консервативные структуры микроорганизмов и активирующие клеточный иммунный ответ. Известно 13 толл-подобных рецепторов млекопитающих, обозначаемых аббревиатурами от TLR1 до TLR13. У человека обнаружено 10 толл-подобных рецепторов (от TLR1 до TLR10). Они играют роль «моста» между врожденным и адаптивным иммунитетом [61].
Благодаря снипам TLR обладают выраженной полиморфность. Dhiman et al. [62] при генотипировании 190 пациентов в возрасте от 12 до 18 лет, обнаружили 6 вариантов снипов в генах TLR. Их роль в иммунных ответах на вакцинацию изучена у пациентов, вакцинированных живой коревой вакциной. Установлено, что гетерозиготные варианты rs3775291 (Phe412Leu) и rs5743305 (−926 п.о. в промоторном регионе гена) TLR3 ассоциированы со слабыми антительными и лимфопролиферативными ответами (p≤0,02) на двукратную вакцинацию коревой вакциной. Гетерозиготные варианты rs4986790 (Gly299Asp) и rs4986791 (Ile399Thr) в гене TLR4 демонстрируют высокий уровень секреции IL-4 (p≤0,02). Гетерозиготные варианты снипов в TLR5 (rs5744174) и TLR6 (rs5743818) ассоциированы с высокими уровнями секреции IFN-γ (p≤0,02).
Рецепторы SLAM (signaling lymphocyte activation molecule) и CD46 (membrane cofactor protein). Рецепторы SLAM расположены на мембране лимфоцитов и стимулирует Т- и В-лимфоциты, рецептор CD46 экспрессируется всеми клетками тканей человека, кроме эритроцитов, и выполняет функцию кофактора фактора комплемента I – сериновой протеазы, которая защищает аутологические клетки против атаки системой комплемента с помощью протеолиза факторов C3b и C4b, прикрепляющихся к ткани. С обоими рецепторами взаимодействует вирус кори. G.A. Poland et al. [63] показали ассоциацию минорных аллелей rs3796504 и rs164288 SLAM-гена с дозозависимым четырехкратным снижением IgG-антител в сыворотке крови детей, вакцинированных живой коревой вакциной. Снип (rs2724384), расположенный в интронном участке гена CD46, ассоциирован с двухкратным дозозависимым снижением IgG-антител в сыворотке крови после вакцинации живой коревой вакциной.
Рецепторы витаминов А (retinoic acid receptor, RAR) и D (vitamin D receptor, VDR). Витамин А (ретинол), витамин D (холекальциферол) и их рецепторы — важные регуляторы иммунных ответов на возбудители инфекционных болезней. Метаболиты витаминов А и D, такие как ретиноевая кислота (retinoic acid) и 1,25-дигидроксивитамин D3 (1,25-dihydroxyvitamin D3), соответственно, обладают самостоятельным иммунорегуляторным действием [64]
Известен один тип рецептора для витамина D — рецептор мембраны ядра клетки VDR/RXRA; и три типа рецепторов ретиноевой кислоты, принадлежащие к семейству ядерных рецепторов для гормонов: α-рецептор ретиноевой кислоты (retinoic acid receptor alpha, RARA), β-рецептор ретиноевой кислоты (retinoic acid receptor beta, RARB) и γ-рецептор ретиноевой кислоты (retinoic acid receptor gamma, RARG) Благодаря наличию снипов в промоторных и интронных областях, гены рецепторов витаминов А и D гетерогенны [64].
Рецептор витамина D образует гетеродимер (heterodimer) с ретиноидным α-X-рецептором клеточного ядра (nuclear retinoid X receptor alpha, RXRA). Посредством рецептора VDR/RXRA модулируются цитокиновые ответы Т-клеток. Мутация в гене, кодирующем мембранный белок, формирующий рецептор, приводит к врожденной низкой усвояемости витамина D. Одновременно этот генотип ассоциируется с повышенным риском развития остеопорозов. Полиморфизмы гена рецептора витамина D связаны с повышенной восприимчивостью к возбудителям инфекций, таким как ВИЧ-1, вирус гепатита В (HBV), человеческий Т-лимфотропный вирус первого типа (HTLV-1) и микобактерии, вызывающие туберкулез [65,66].
Установлено статистически достоверное снижение выраженности гуморальных (титры специфических антител в сыворотке крови) и клеточных иммунных ответов (содержание IL-2, IL-6, IL-10, IFN-α, IFN-γ и TNF-α в сыворотке крови) на коревую вакцину у здоровых детей белой расы, с поврежденными снипами генами рецепторов витаминов А и D [64].
Врожденная недостаточность функции фагоцитоза. В хромосоме 2q35 человека идентифицирован ген NRAMP1 (natural resistance-associated macrophage protein gene 1, другое название SLC11A1), гомологичный мышиному Bcg-гену, который придает мышам резистентность к бациллам Кальмета–Герена и к возбудителю лепры. Биохимическая функция белка полностью не ясна, но есть основания считать, что он способствует функции фагоцитоза у макрофагов и «представлению» ими антигенов Т-хелперам. Первые прямые доказательства причастности мутантных аллелей этого гена к развитию проказы получены при изучении эпидемиологии болезни среди населения Южного Вьетнама [67]. Отдельные аллели гена с высокой частотой преобладают в восточно-африканской популяции, но редко встречаются в европейских. Это наблюдение может частично объяснить более высокую, в сравнении с другими этническими группами, чувствительность восточных африканцев к туберкулезу [65]. Нетранслируемый ген NRAMP1 у жителей Гамбии ассоциируется с открытыми формами легочного туберкулеза и, следовательно, с передачей M. tuberculosis по эпидемической цепочке — от одного заболевшего к другому [19]. Установлена ассоциация N02C-аллели NRAMP1 у детей различных этнических групп, живущих в Большом Хьюстоне (США), со злокачественным течением туберкулеза [68]. Выявлена ассоциация мутантных аллелей этого гена с диссеминацией у детей вакцины BCG [69].
Маннозасвязывающий лектин (mannose-binding lectin 2, MBL2). Кальцийзависимый маннозасвязывающий лектин сыворотки крови связывается с терминальными маннозными группами на поверхности различных бактерий и вирусов. Тем самым он инициирует активацию комплемента (классический путь) и механизм опосонофагоцитоза (opsonophagocytosis), независящего от антител и Clq (одна из трех субъединиц белка Cl комплемента, в ее составе имеется рецептор для связывания с Fc-фрагментом антитела). Мутация в экзоне 1 MBL2 снижает концентрацию MBL в сыворотке, вероятно вследствие интерференции с олигомеризованным белком. Низкие уровни MBL могут быть связаны с рекуррентными инфекциями у детей. Мутация в экзоне 1 у отдельных этнических групп ассоциируется с менингеальным туберкулезом [70]. Pöyhönen et al [71] получили данные, позволяющие им предположить, что низкое содержание MBL в сыворотке крови детей ассоциировано с риском развития у них BCG-остеитов.
Приведенные данные показывают фрагментарную изученность роли отдельных аллелей генов человека в ответах иммунной системы на возбудители инфекционной болезни или вакцинацию. В тоже время участие отдельных генов в иммунных ответах может носить универсальный характер (TNF*2, NRAMP1 и др.). Полиморфизмы генов IL1, IL4 или IL18 являются причиной сходных поствакцинальных осложнений у пациентов после иммунизации MMR-вакциной, живой оспенной вакциной и др. [50,51,52,]. Поэтому в табл. 5 нами указана помимо известной, еще и их возможная ассоциация с осложнениями, развивающимися после вакцинации.
Таблица 5
Аллели генов, участвующих в регуляции иммунного ответа у человека и возможная их ассоциация с осложнениями, возникающими после вакцинации
|
Аллель |
Нарушение иммунного ответа |
Установленные осложнения при инфекционном или поствакцинальном процессах |
Возможные осложнения после вакцинации |
|
МНС II DRB1*11 |
Пониженная секреция интерферона-гама и IL-2 макрофагами в ответ на антигенную стимуляцию |
Переход острой стадии Ку-лихорадки в хроническую, развитие эндокардитов |
Развитие эндокардитов после вакцинации живыми вакцинами |
|
МНСI A1-B8-DR3 |
Повышенная продукция TNF макрофагами в ответ на инфекцию |
Развитие шока при инфицировании хантавирусом Puumala |
Развитие шоковых состояний в ответ на введение инактивированных и химических вакцин, развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами |
|
МНСII DR2 и DR |
Нарушение Т-клеточного ответа на микобактерии |
Ассоциируются с легочным туберкулезом и туберкулоидной проказой |
Генерализация BCG |
|
МНСII DRB1*03, DQA1*0201, DRB1*07–DQB1*02–DPB1*02, DRB1*07–DQB1*03–DPB1*04 и МНСI B8, B13 и B44, В58 |
Недостаточность системы гуморального иммунитета |
Низкий титр специфических антител после однократной вакцинации живой коревой вакциной |
Слабые ответы со стороны системы гуморального иммунитета на введение вакцин любого типа |
|
МНСII DQB1*0303 |
То же |
Низкий титр специфических антител после однократной вакцинации живой паротитной вакциной |
То же |
|
МНСI A(*2402 и *6801) |
Недостаточность системы клеточного иммунитета |
Ассоциированы с низким содержанием в сыворотке крови IFN-γ в ответ на вакцинацию живой вакциной против краснухи |
Слабые ответы со стороны системы клеточного иммунитета на введение вакцин любого типа |
|
МНСII DQB1*0603–9/14 |
Недостаточность системы гуморального иммунитета |
Антител в ответ на вакцинацию субъединичными гриппозными вакцинами не образовывалось |
Слабые ответы со стороны системы гуморального иммунитета на введение вакцин любого типа |
|
МНСI: B*3701 B*4001, B*5301, B*5601, C*0102, C*0702 и C*0801 |
Недостаточность системы клеточного иммунитета
|
Низкие уровни в сыворотке крови IFN-γ в ответ на вакцинацию живой оспенной вакциной Dryvax™ |
Слабые ответы со стороны системы клеточного иммунитета на введение вакцин любого типа |
|
МНСII DRB1*03, DRB1*07 и DQB1*03 |
Недостаточность системы гуморального иммунитета |
Антитела в ответ на введение вакцины против гепатита В не образуются |
Слабые ответы со стороны системы гуморального иммунитета на введение вакцин любого типа, хронизация инфекционных процессов |
|
TNF*2 |
Более сильный транскрипционный активатор, способствующий увеличению экспрессии TNFα |
Развитие церебральных форм малярии, развитие шока в ответ на инфекцию, вызванную хантавирусом, быстрое прогрессирование проказы и легочной формы туберкулеза, фатальные исходы менингококковых инфекций |
Развитие шоковых состояний в ответ на введение инактивированных и химических вакцин, развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами |
|
TNFα, IL1R, IL6, IL10, IL12RB2, IL12RB2 и IL12RB1 |
Снипы, подавляющие экспрессию генов |
Слабые гуморальные и клеточные ответы на введение живых коревой и паротитной вакцин |
Слабые ответы со стороны систем гуморального и клеточного иммунитета на введение вакцин любого типа |
|
IL-2, IL-2Rγ, IL-12, IL-12RB1 |
То же |
Генерализация вакцины BCG |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, |
|
IL1, IL4, IL18 |
Снипы, усиливающие экспрессию генов |
Развитие лихорадки (t≥37,7°C) и миокардита у пациентов, вакцинированных оспенной вакциной DryvaxTM |
Осложнения в виде лихорадочных реакций на введение живых вакцин |
|
NRAMP1 |
Врожденная недостаточность функции фагоцитоза |
Высокая чувствительность к туберкулезу, развитие открытых форм легочного туберкулеза, злокачественное течение туберкулеза |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
|
IFN-γ R1 |
Врожденная недостаточность системы интерферона |
Диссеминация малопатогенных микобактерий, развитие фатального лептоменингита после вакцинации BCG, развитие BCG -остеомиелитов |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
|
VDR |
Врожденная низкая усвояемость витамина D |
Повышенная восприимчивость к ВИЧ-1, HBV, HTLV-1 и микобактериям. Развитие легочной формы туберкулеза и остеопороза |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
|
TLR3 (гетерозиготные варианты rs3775291 и rs5743305) |
Снипы, подавляющие экспрессию генов |
Слабые гуморальные и клеточные ответы на введение живой коревой вакцины |
Слабые ответы со стороны систем гуморального и клеточного иммунитета на введение вакцин любого типа |
|
SLAM и CD46 |
То же |
Слабые гуморальные ответы на введение живой коревой вакцины |
Слабые ответы со стороны системы гуморального иммунитета на введение вакцин любого типа |
|
MBL2 (мутация в экзоне 1) |
Снижение концентрации MBL в сыворотке |
Повышенная чувствительность к возбудителям рекуррентных инфекций у детей. У отдельных этнических групп ассоциируется с туберкулезом менингеальных оболочек. Повышенный риск развития BCG-остеитов |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
***
Динамика эпидемического процесса, наиболее характерная для него клиническая картина болезни, эффективность и безопасность вакцинации, частота поствакцинальных осложнений, среди прочих факторов[13] находятся в тесной зависимости от относительного количества в популяции лиц с дефектами (полиморфизмами) генов иммунной системы и систем, участвующих в патогенезе болезни. Полиморфизация таких генов происходит спонтанно, в результате образования снипов и делеций, распределяющихся в следующих поколениях в соответствии с законами Менделя. Снятие селективного давления на популяции людей со стороны возбудителей контагиозных циклических инфекций, одновременно устранило механизмы, ограничивающие этот процесс. Темпы накопления полиморфизмов возрастают в относительно генетически однородных популяциях (жители островных государств), и в популяциях, практикующих браки между родственниками.
Иммунизация живой коревой вакциной малоэффективна у индивидуумов с МНС I B8, B13, B44, B58; МНС II DRB1*03, DQA1*0201 DRB1*07–DQB1*02–DPB1*02 и DRB1*07–DQB1*03–DPB1*04; снипами в генах, кодирующих рецепторы TLR3 (rs164288, rs3775291, rs3796504, rs5743305), SLAM (rs2724384) и CD46.
Иммунизация живой паротитной вакциной малоэффективна у индивидуумов с МНС II DQB1*0303 и снипами в генах IL12RB2, IL12RB1, IL10 и IL12RB2.
Иммунизация живой вакциной против краснухи малоэффективна у индивидуумов с МНС-A (*2402 и *6801).
Иммунизация вакциной против гепатита В малоэффективна у индивидуумов с МНС II DRB1*03, DRB1*07 и DQB1*03.
Иммунизация гриппозными вакцинами малоэффективна у индивидуумов с МНС DQB1*0603–9/14.
Осложнения после вакцинации живой оспенной вакциной возможны у индивидуумов с МНС класса I: B*3701, B*4001, B*5301, B*5601, C*0102, C*0702 и C*0801 и с отдельными гаплотипами IL1, IL18.
Диссеминация туберкулезной вакцины на основе штамма BCG у ребенка возможна при наличии снипов и делеций в генах: NRAMP1, MBL (развитие BCG-остеита), витамина D, IL-2, IL-12, IFN-γ и их рецепторов.
Расследование случаев поствакцинальных осложнений должно проводиться с учетом причастности генетического фактора, включая помимо генов иммунной системы, выявление влияния на патогенез инфекционной болезни генетических дефектных физиологических систем организма человека.
Литература
1. Ясинский АА, Михеева ИВ. Безопасность иммунизации. В кн.: Зверев ВВ, Семенов БФ, Хаитов РМ, ред. Вакцины и вакцинация. Национальное руководство. М.: 2011. С. 137–61.
2. Blackwell JM, Jamieson SF, Burgner D. HLA and Infectious Diseases. Clinical Microbiology Reviews 2009; 22(2): 370–85.
3. Петухов ВЛ, Жигачев АИ, Назарова ГА. Ветеринарная генетика. М.: 1996.
4. Hill A. Genetics of infectious disease. Phil Trans R Soc B. 2012; 367: 840–9.
5. Губерт ВО. Оспа и оспопрививание. СПб.: 1896.
6. Downie AW, McCarthy K. The antibody response in man following infection with viruses of the pox group. III. Antibody response in smallpox. J Hyg. (London) 1958; 56: 479–87.
7. Rumyantsev SN. The origin of individual differences in the course and severity of diseases. The Sci World J. 2006; 6: 1674–704.
8. Poland GA, Ovsyannikova IG, Jacobson RM. Vaccine immunogenetics: bedside to bench to population. Vaccine 2008; 26(49): 6183–8.
9. Marquet S, Schurr E. Genetics of susceptibility to infectious diseases: tuberculosis and leprosy as examples. Drug Metabolism and Disposition 2001; 29(4): 478–83.
10. Rasmussen AL, Okumura A, Ferris MT, Green R, Feldmann F, Kelly SM et al. Host genetic diversity enables Ebola hemorrhagic fever pathogenesis and resistance. Science 2014; 346(6212): 987-91.
11. Blackwell JM, Jamieson SF, Burgner D. HLA and Infectious Diseases. Clinical Microbiology Reviews 2009; 22(2): 370–85.
12. Галактионов В Г. Иммунология. М.: 1998.
13, Коротяев АИ, Бабичев СА. Медицинская микробиология, иммунология и вирусология. СПб.: 1998.
14. Короткова ИЮ. Клиническая иммуногенетика заболеваний, злокачественных новообразований и хронических воспалительных процессов: автореф. дис. …д-ра мед. наук. Новосибирск. 2007.
15. Бухарин ОВ, Усвяцов Б.Я. Бактерионосительство. Екатеринбург. 1996.
16. Singh N, Agrawal S, Rastogi A. Infectious diseases and immunity: Special reference to major histocompatability complex. Emerging Infectious Diseases1997; 3(1): 24–34.
17. Helbig K, Harris R, Ayres J, Dunckley H, Lloyd A, Robson J, Marmion BP. Immune response genes in the post-Q-fever fatigue syndrome, Q fever endocarditis and uncomplicated acute primary Q fever. Q J Med. 2005; 98: 565–74.
18. Hill A, Elvin J, Will A, Aidoo M, Allsopp CE, Gotch FM et al. Molecular analysis of the association of HLA-B53 and resistance to severe malaria. Nature 1992; 360: 434–9.
19. Hill A. Genetics and genomics of infectious disease susceptibility. British Medical Bulletin 1999; 55(2): 401–13.
20. Wilson A, Symons J, McDowell T, McDevitt HO, Duff GW. Effects of polymorphism in the tumor necrosis factor alpha promoter on transcriptional activation. Proc Natl Acad Sci USA 1997; 94(10): 3195–9.
21. Kalish RA, Leong JM, Steere AC. Association of treatment-resistant chronic Lyme arthritis with HLA-DR4 and antibody reactivity to OspA and OspB of Borrelia burgdorferi. Infect Immun. 1993; 61(7): 2774-9.
22. Fitness J, Tosh K, Hill A. Genetics of susceptibility to leprosy. Genes and Immunity 2002; 3: 441–53.
23. Singh N, Agrawal S, Rastogi A. Infectious diseases and immunity: Special reference to major histocompatability complex. Emerging Infectious Diseases1997; 3(1): 24–34.
24. Захарычева ТА, Колотушкина ГБ, Жукова СГ, Сай ИА. Антигены системы HLA у больных различными формами клещевого энцефалита в хабаровском крае. В кн.: Нейроиммунология. Юбилейная X конференция. 28-31 мая 2001 г. Том 2; С. 223–97.
25. Poland GA, Ovsyannikova IG, Jacobson RM, Vierkant RA, Jacobsen SJ, Pankratz VS, Schaid DJ. Identification of an association between HLA class II alleles and low antibody levels after measles immunization. Vaccine 2001; 20: 430–8.
26. Jacobson RM, Poland GA, Vierkant RA, Pankratzd V, Schaidd DJ, Jacobsene SJ et al. The association of class I HLA alleles and antibody levels following a single dose of measles vaccine. Hum Immunol. 2003; 64: 103–9.
27. Ovsyannikova IG, Jacobson RM, Vierkant RA, Shane Pankratz V, Jacobsen SJ, Poland GA. Associations between human leukocyte antigen (HLA) alleles and very high levels of measles antibody following vaccination. Vaccine 2004; 22: 1914–20.
28. Ovsyannikova IG, Jacobson RM, Vierkant RA, Pankratz VS, Poland GA. HLA supertypes and immune responses to measles–mumps–rubella viral vaccine: findings and implications for vaccine design. Vaccine 2007а; 25: 3090–100.
29. Ovsyannikova IG, Pankratz SV, Vierkant R, Jacobson RM, Poland GA. Human leukocyte antigen haplotypes in the genetic control of immune response to measles–mumps–rubella vaccine. J Infect Dis. 2006; 193: 655–63.
30. Ovsyannikova IG, Jacobson RM, Dhiman N, Vierkant RA, Pankratz VS, Poland GA. Human leukocyte antigen and cytokine receptor gene polymorphisms associated with heterogeneous immune responses to mumps viral vaccine. Pediatrics 2008; 121: 1091–9.
31. Ovsyannikova IG, Jacobson RM, Ryan JE et al. Relationship between HLA polymorphisms and γ-interferon and interleukin-10 cytokine production in healthy individuals after rubella vaccination. Clin Vaccine Immunol. 2007б; 14: 115–22.
32. Poland GA, Ovsyannikova IG, Jacobson RM Application of pharmacogenomics to vaccines. Pharmacogenomics 2009; 10(5): 837–52.
33. Poland GA, Ovsyannikova IG, Jacobson RM. Immunogenetics of seasonal influenza vaccine response. Vaccine 2008а; 26: 35–40.
34. Poland GA, Ovsyannikova IG, Jacobson RM. Immunogenetics of seasonal influenza vaccine response. Vaccine 2008б; 26: 6183–8.
35. Gelder CM, Lambkin R, Hart KW, Fleming D, Williams OM, Bunce M et al. Associations between human leukocyte antigens and nonresponsiveness to influenza vaccine. J Infect Dis. 2002; 185: 114–7.
36. Ovsyannikova IG, Jacobson RM, Targonski PV et al. Vaccine Congress. Amsterdam: The Netherlands; 2007в. Influence of host genetic variation on the immune response to the smallpox vaccine; p. 9-11. Abstract O33.
37. Willems A, Leroux-Roels G. Response to hepatitis B vaccine: multiple HLA genes are involved. Tissue Antigens 1998; 51(6): 593–604.
38. Poland GA, Ovsyannikova IG, Jacobson RM, Vierkant RA, Jacobsen SJ, Pankratz VS, Schaid DJ. Identification of an association between HLA class II alleles and low antibody levels after measles immunization. Vaccine 2001; 20: 430–8.
39. Wang C, Tang J, Song W, Lobashevsky E, Wilson CM, Kaslow RA. HLA and cytokine gene polymorphisms are independently associated with responses to hepatitis B vaccination. Hepatology 2004; 39(4): 978–88.
40. Thursz M. Pros and cons of genetic association studies in hepatitis B. Hepatology 2004; 40(2): 284–6.
41. Engele M, Stossel E, Castiglione K, Schwerdtner N, Wagner W, Bölcskei P et al. Induction of TNF in human alveolar macrophages as a potential evasion mechanism of virulent Mycobacterium tuberculosis. J Immunol. 2002; 168: 1328–37.
42. Cabrera M, Shaw MA, Sharples C, Williams H, Castes M, Convit J et al. Polymorphism in tumor necrosis factor genes associated with mucocutaneous leishmaniasis. J Exp Med. 1995; 182: 1259–64.
43. Conway DJ, Holland MJ, Bailey RL. Campbell AE, Mahdi OSM, Jennings R. et al. Scarring trachoma is associated with polymorphism in the tumor necrosis factor alpha (TNF-alpha) gene promoter and with elevated TNFalpha levels in tear fluid. Infect Immun. 1997; 65: 1003–6.
44. McGuire W, Hill A, Allsopp C, Greenwood BM, Kwiatkowski D. Variation in the TNF-a promoter region associated with susceptibility to cerebral malaria. Nature 1994; 371: 508–11.
45. Nadal D, Leppert D, Frei K, Gallo P, Lamche H, Fontana A. Tumour necrosis factor-alpha in infectious meningitis. Arch Dis Child. 1989; 64: 1274–9.
46. Wilson A, Symons J, McDowell T, McDevitt HO, Duff GW. Effects of polymorphism in the tumor necrosis factor alpha promoter on transcriptional activation. Proc Natl Acad Sci USA 1997; 94(10): 3195–9.
47. Shaw MA, Donaldson IJ, Collins A, Peacock CS, Lins-Lainson Z, Shaw JJ et al. Association and linkage of leprosy phenotypes with HLA class II and tumour necrosis factor genes. Genes Immun. 2001; 2: 196–204.
48. Dhiman N, Ovsyannikova IG, Vierkant RA, Pankratz VS, Jacobson RM, Poland GA. Associations between cytokine/cytokine receptor SNPs and humoral immunity to measles, mumps and rubella in a Somali population. Tissue Antigens 2008; 72: 211–20.
49. Dhiman N, Ovsyannikova IG, Cunningham JM, Robert A. Vierkantc, V. Pankratzc S, Jacobson RM et al. Associations between measles vaccine immunity and single nucleotide polymorphisms in cytokine and cytokine receptor genes. J Infect Dis 2007а; 195: 21–9.
50. Stanley SL Jr, Frey SE, Taillon-Miller P, Guo J, Miller RD, Koboldt DC et al. The immunogenetics of smallpox vaccination. J Infect Dis. 2007; 196: 212–219.
51. Usonis V, Bakasenas V, Kaufhold A, Chitour K, Clemens R. Reactogenicity and immunogenicity of a new live attenuated combined measles, mumps and rubella vaccine in healthy children. Pediatr Infect Dis. J. 1999; 18: 42–48.
52. Vestergaard M, Hviid A, Madsen KM, Wohlfahrt J, Thorsen P, Schendel D, Melbye M, Olsen J. MMR vaccination and febrile seizures: evaluation of susceptible subgroups and long-term prognosis. JAMA. 2004; 292: 351–7.
53. Altare F, Lammas D, Revy P, Jouanguy E, Döffinger R, Lamhamedi S et al. Inherited Interleukin 12 deficiency in a child with bacille Calmette-Guerin and Salmonella enteritidis disseminated Infection. J Clin Invest. 1998; 102(12): 2035–40.
54. Elloumi-Zghal H, Ridha Barbouche M, Chemli J, Bejaoui M, Harbi A, Snoussi N, Abdelhak S, Dellagi K. Clinical and genetic heterogeneity of inherited autosomal recessive susceptibility to disseminated Mycobacterium bovis Bacille Calmette-Guerin infection. The Journal of Infectious Diseases 2002; 185: 1468–75.
55. Li-Hsin H, Shyh-Dar S, Jyh-Der W, Shin-Chi, Chin-Yuan T, Fu-Yuan H. Disseminated bacille Calmette-Guerin disease as the initial presentation of X-linked severe combined Immunode-ficiency. A case report. Asian Pacific Journal of Allergy and Immunology 2005; 23: 221-6.
56. Marquet S, Schurr E. Genetics of susceptibility to infectious diseases: tuberculosis and leprosy as examples. Drug Metabolism and Disposition 2001; 29(4): 478–83.
57. Jouanguy E, Lamhamedi-Cherradi S, Lammas D et al. A human IFNGR1 small deletion hotspot associated with dominant susceptibility to mycobacterial infection. Nat Genet 1999; 21: 370–8.
58. Jouanguy E, Lamhamedi-Cherradi S, Altare F, Fondaneche MC, Tuerlinckx D, Blanche S et al. Partial interferon-γ receptor 1 deficiency in a child with tuberculoid Bacillus Calmette-Guerin infection and a sibling with clinical tuberculosis. J Clin Invest. 1997; 100(11): 2658–64.
59. Sasaki Y, Nomura A, Kusuhara K, Takada H, Ahmed S, Obinata K, Hamada K, Okimoto Y, Hara T. Genetic basis of patients with bacille Calmette-Guerin osteomyelitis in Japan: identification of dominant partial interferon-γ receptor 1 deficiency as a predominant type. J Infect Dis. 2002; 185: 706–9.
60. Reif DM, McKinney BA, Motsinger AA, Chanock SJ, Edwards KM, Rock MT, Moore JH et al. Genetic basis for adverse events after smallpox vaccination. J Infect Dis. 2008; 198: 1–7.
61. Dhiman N, Ovsyannikova IG, Vierkant RA, Pankratz VS, Jacobson RM, Poland GA. Associations between cytokine/cytokine receptor SNPs and humoral immunity to measles, mumps and rubella in a Somali population. Tissue Antigens 2008б; 72: 211–20.
62. Dhiman N, Ovsyannikova IG, Vierkant RA et al. Associations between SNPs in toll-like receptors and related intracellular signaling molecules and immune responses to measles vaccine: preliminary results. Vaccine 2008; 26: 1731–36.
63. Poland GA, Ovsyannikova IG, Jacobson RM Application of pharmacogenomics to vaccines. Pharmacogenomics 2009; 10(5): 837–52.
64. Ovsyannikova IG, Haralambieva IH, Vierkant RA, O'Byrne MM, Jacobson RM, Poland GA. Effects of vitamin A and D receptor gene polymorphisms/haplotypes on immune responses to measles vaccine. Pharmacogenet Genomics 2012; 22(1): 20–31.
65. McNicholl J, Smith DK, Qari S, Hodge T. Host genes and HIV: the role of the chemokine receptor gene CCR5 and its allele. Emerging Infectious diseases 1997; 3(3): 261–72.
66. Bellamy R, Ruwende C, Corrah T, McAdam KPWJ, Thursz M, Whittle HC, Hill AVS. Tuberculosis and chronic hepatitis B virus infection in africans and variation in the vitamin D receptor gene. The Journal of Infectious Diseases 1999; 179: 721–4.
67. Abel L, Vu DL, Oberti J, Nguyen VT, Van VC, Guilloud-Bataille M, Schurr E, Lagrange PH et al. Complex segregation analysis of leprosy in southern Vietnam. Genet Epidemiol. 1995; 12: 63–82.
68. Malik S, Abel L, Tooker H, Poon A, Simkin L, Girard M et al. Alleles of the NRAMP1 gene are risk factors for pediatric tuberculosis disease. Proc Natl Acad Sci USA 2005; 102(34): 12183–8.
69. Alm J, Sanjeevi CB, Miller EN, Dabadghao P, Lilja G, Pershagen G et al. Atopy in children in relation to BCG vaccination and genetic polymorphisms at SLC11A1 (formerly NRAMP1) and D2S1471. Genes and Immunity. 2002; 3: 71–7.
70. Hoal-Van H, Epstein J, Victor T, Hon D, Lewis LA, Beyers N et al. Mannosebinding protein B allele confers protection against tuberculous meningitis. Pediatr Res. 1999; 45(Pt 1): 459–64.
71. Pöyhönen L, Kröger L, Gröndahl-Yli-Hannuksela K, Vuononvirta J, Huhtala H, He Q, Korppi M. Variant MBL2 genotypes producing low mannose-binding lectin may increase risk of Bacillus Calmette-Guerin osteitis in vaccinated newborns. Acta Paediatr. 2013; 102(11): 1095-9.
Библиографическое описание: Супотницкий МВ. Генетические ограничения эффективности и безопасности массовых вакцинаций населения Актуальная инфектология 2015; (1): 100–15.
Bibliographical description: Supotnitskiy МV. Genetic-associated reduced efficiency and safety of cohort immunization. Actual Infectology 2015; (1): 100–15.
Библиографическое описание: Супотницький МВ. Генетичні обмеження ефективності та безпеки масових вакцинацій населення. Актуальна iнфектологiя 2015; (1): 100–15.
[1]Hill [4] называет это явление генетической архитектурой чувствительности к инфекционной болезни.
[2]См. ниже «Главный комплекс гистосовместимости»
[3]Гистосовместимость — совместимость органов и тканей, например, при трансплантации совместимая ткань не отторгается организмом реципиента. Определяется специфическими антигенными комплексами МНС. Историческое называние МНС — «человеческий лейкоцитарный антиген» (human leucocyte antigen, HLA).
[4] Гаплотип — совокупность аллелей на локусах одной хромосомы, обычно наследуемых вместе.
[5]В геноме человека обнаружено 1,42 млн снипов, примерно 60 тыс. из них локализованы в кодирующих областях генов.
[6]Взято с сайта http://2146777.ru/articles.php?id=31.
[7]Обстоятельно данная проблема рассмотрена в работе И.Ю.Коротковой [14] на примере населения Западной Сибири.
[8]Вакцина MMR — лиофилизированный препарат, содержащий ослабленные вирусы кори, паротита и краснухи. Вирусы, входящие в состав вакцины идентичны вирусам, используемым для производства ATTENUVAX (живая коревая вакцина, MSD), MUMPSVAX (живая вакцина против паротита, MSD) и MERUVAX II (живая вакцина против краснухи, MSD). Три вируса смешивают перед лиофилизацией.
[9]В России эта вакцина не зарегистрирована.
[10]Такие процессы называются транзициями — это мутация замены оснований, когда одно пуриновое основание замещается на другое пуриновое основание (аденин на гуанин или наоборот).
[11]Метилентетрагидрофолатредуктаза (methylenetetrahydrofolate reductase, MTHFR) — внутриклеточный фермент, играющий ключевую роль в метаболизме фолата и метионина. Необратимо преобразует 5,10-метилентетрагидрофолат в 5-метилтетрагидрофолат.
[12]Факторы регуляции интерферонов (interferon regulatory factors, IRF) — белки, регулирующие транскрипцию интерферонов. IRF1 — транскрипционный активатор гена β-интерферона.
[13] Среди этих факторов наиболее существенны вирулентность возбудителя инфекционной болезни, наличие переносчиков возбудителя, наличие вакцинированной прослойки, параллельно протекающих эпидемических процессов, например, ВИЧ/СПИДа, Т-клеточного лейкоза, герпеса 1 и 2 типов.

Михаил Васильевич Супотницкий
Российский микробиолог, полковник медицинской службы запаса, изобретатель, автор книг и статей по истории эпидемий чумы и других особо опасных инфекций, истории разработки и применения химического и биологического оружия. Заместитель главного редактора научно-практического журнала «Вестник войск РХБ защиты» Министерства обороны РФ.