Основные технологические процессы, используемые при производстве биомедицинских клеточных продуктов
(в соавторстве с Елаповым АА, Меркуловым ВА, Борисевичем ИВ, Климовым ВИ, МироновымАН)
Получение специфичных, эффективных и безопасных биомедицинских клеточных продуктов (БМКП) предполагает осуществление следующих типовых операций: а) получение клеточной линии определенного клеточного состава; б) наработка клеток определенной клеточной линии в количествах, необходимых для терапевтического применения в составе БМКП; в) контроль качества и стандартизация полученной клеточной линии. Наиболее предпочтительными для целей клеточной терапии специалисты считают мезенхимальные стромальные клетки (МСК). Получение клеточной линии определенного клеточного состава включает пять последовательно выполняемых этапов: отбор донора, отбор биологического материала, выделение клеток из материала донора, получение стандартизуемой популяции однородных клеток, охарактеризование клеточного состава клеточной линии и ее паспортизация. Процесс наработки клеточной линии в количествах, позволяющих их терапевтическое применение в составе БМКП, включает подбор питательной среды для выращивания МСК, культивирование в специальных биореакторах, контроль параметров культивирования. Контроль качества и стандартизация полученной клеточной линии предполагает разработку общих требований к показателям качества, применимых ко всем клеточным линиям; и частных, которые будут использоваться для оценки терапевтических препаратов, имеющих свой круг показаний (например, для лечения сахарного диабета, костной пластики, восстановление кровоснабжения ишемизированного миокарда). В статье на основе анализа научной литературы и патентов, впервые приведено описание контрольных точек типовых операций и основных технологических приемов, используемых при производстве БМКП и оценке их качества, которые должны быть в поле зрения экспертов контрольного органа; сформулированы требования к содержанию документации, представляемой разработчиком БМКП в регистрационном досье в контрольный орган.
Библиографическое описание: Супотницкий МВ, Елапов АА, Меркулов ВА, Борисевич ИВ, Климов ВИ, Миронов АН. Основные технологические процессы, используемые при производстве биомедицинских клеточных продуктов. Биопрепараты 2015; (2): 36–45.
Developing specific, effective and safe biomedical cell culture products (BCCP) assumes the following standard operating procedures: a) developing cell line with specific cell composition; b) obtaining a sufficient amount of cells of a specific cell line for therapeutic use as a part of BCCP; c) quality control and standardization of the developed cell line. Experts believe mesenchymal stromal cells (MSC) to be the first choice for the purpose of stem cell therapy. The development of a cell line with a specific cellular composition includes five sequential steps: selection of donors, sampling of biological material, cell isolation from donor material, preparation of standardized homogeneous population of cells, characterization of cell line composition of the cell line and its certification. The process of obtaining a sufficient amount of cells of a specific cell line for therapeutic use as a part of BCCP includes the selection of culture medium for cultivation of MSC, in special bioreactors for cultivation and culture control parameters. Quality control and standardization of the developed cell line assumes the elaboration of general requirements for quality parameters, characterizing all cell lines; as well as specific requirements for the assessment of therapeutic preparations in accordance with their proposed indications (for example, for the treatment of diabetes, bone grafting, restoration of blood supply to ischemic myocardium). The article describes typical procedures and identifies possible checkpoints for common technological methods used in BCCP manufacture and their quality assessment. It also outlines the requirements for the content of documents submitted by BCCP developer to an official authority in marketing authorization dossier as well as the expert evaluation procedure.
Bibliographic description: Supotnitskiy MV, Elapov AA, Merkulov VA, Borisevich IV, Klimov VI, Mironov AN. Common technological processes used in manufacture of biomedical cell culture products. Biopreparation (Biopharmaceuticals) 2015; (2): 36–45.
Биомедицинские клеточные продукты (БМКП) – новые перспективные средства профилактики, диагностики и лечения заболеваний (патологических состояний), сохранения беременности и медицинской реабилитации пациента. Их использование позволяет восстанавливать структуру и функцию тканей и органов человека, активировать восстановительные процессы организма человека (регенеративная терапия), создавать ткани и органы биоинженерными методами (тканевая инженерия), адресно доставлять лекарственные препараты в организм человека [1]. Цель данной работы – определить основные технологические процессы, используемые при производстве биомедицинских клеточных продуктов.
Получение специфичных, эффективных и безопасных БМКП предполагает осуществление следующих типовых операций: а) получение клеточной линии определенного клеточного состава; б) наработка клеток определенной клеточной линии в количествах, необходимых для терапевтического применения в составе БМКП; в) контроль качества и стандартизация полученной клеточной линии [2, 3].
Получение клеточной линии определенного клеточного состава
К клеточной линии, способной дифференцироваться в направлении определенного исследователем клеточного типа, относятся линии, сформированные стволовыми клетками (stem cells), т.е. недифференцированными клетками, являющимися клональными предшественниками специализированных клеток, формирующих органы и ткани. В настоящее время обнаружены несколько типов стволовых клеток, которые могут быть использованы для разработки БМКП (рис. 1) [2].
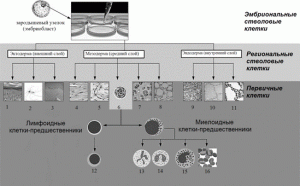 Рис. 1. Типы стволовых клеток, которые могут быть использованы для разработки БМКП^ 1 – клетки кожи; 2 – нейроны; 3 – пигментные клетки; 4 – сердечная мышца; 5 – клетки костной ткани; 6 – гемопоэтические стволовые клетки; 7 – клетки ткани сустава; 8 – трубчатые клетки; 9 – клетки поджелудочной железы; 10 – клетки щитовидной железы; 11 – клетки легкого; 12 – лимфоциты; 13, 14, 15 – различные миелоидные линии; 16 – эритроциты [2].
Рис. 1. Типы стволовых клеток, которые могут быть использованы для разработки БМКП^ 1 – клетки кожи; 2 – нейроны; 3 – пигментные клетки; 4 – сердечная мышца; 5 – клетки костной ткани; 6 – гемопоэтические стволовые клетки; 7 – клетки ткани сустава; 8 – трубчатые клетки; 9 – клетки поджелудочной железы; 10 – клетки щитовидной железы; 11 – клетки легкого; 12 – лимфоциты; 13, 14, 15 – различные миелоидные линии; 16 – эритроциты [2].
Эмбриональные стволовые клетки (embryonic stem cells, ESCs) – клетки ранней стадии эмбрионального развития (до формирования бластоцисты). Для них характерно неограниченное размножение и плюрипотентность, т.е. они способны дифференцироваться в любые типы клеток, происходящие из трех зародышевых листков. Их использование в клинической практике ориентировано на лечение патологических состояний, при которых ограничивающим фактором является гистосовместимость тканей. Однако контролировать дифференцировку таких клеток в ткани реципиента сложно, и они могут стать источником формирования тератом. В соответствие с п. 8. ст. 4 Проекта Федерального закона № 717040-6 от 06.02.2015 г. «О биомедицинских клеточных продуктах», использование таких клеток для получения БМКП в России будет запрещено [1].
Региональные стволовые клетки (somatic stem cells, соматические стволовые клетки; adult stem cells, стволовые клетки взрослых) – полипотентные клетки, способные дифференцироваться только в клетки, происходящие из зародышевого листка, например, мезенхимальные стромальные клетки (mesenchymal stem cells, MSCs, МСК), гемопоэтические стволовые клетки (haemopoietic stem cells, HSCs) и др. Такие клетки содержатся во всех тканях и выполняют функцию клеточного резерва, позволяющего замещать поврежденные дифференцированные клетки. В отличие от плюрипотентных стволовых клеток имеют стойкие биомаркеры, отличающие их потомство от клеток других типов. Кроме того, их способность к пролиферации значительно ниже, чем у плюрипотентных стволовых клеток. Они не создают иммунологических проблем и их дифференцировкой управлять значительно проще, чем дифференцировкой эмбриональных стволовых клеток.
Использование региональных стволовых клеток в медицине сопряжено с рядом трудностей: они медленно растут в питательных средах; процесс их дифференцировки длителен; такие клетки трудно получить в количествах, достаточных для терапевтического применения; на направлении дифференцировки в условиях ex vivo сказывается источник их получения; возможно сокращение длины теломер клеток-трансплантатов, что приводит к раннему старению дифференцировавшихся клеток в реципиентных тканях или к их злокачественному перерождению; такие клетки могут нести реципиенту генетические дефекты, имеющиеся у их донора [4, 5].
Первичные или унипотентные клетки (primary cells, unipotent cell) – региональные стволовые клетки на стадии дифференцировки, предшествующей формированию клеток специализированного типа. Например, лимфоидные клетки-предшественники (lymphoid progenitor cells) дифференцируются в лимфоциты, миелоидные клетки-предшественники (myeloid progenitor cells) – в клетки миелоидной ткани, гоноциты (первичные половые клетки, gonocytes) – в сперматозоиды или яйцеклетки.
Наиболее предпочтительными для целей клеточной терапии специалисты считают региональные стволовые клетки и, в частности, одну из их разновидностей – МСК [2–6].
МСК представляют собой фибробластоподобные клетки, изолированные из костного мозга, жировой и других васкуляризированных тканей. По морфологическим особенностям их относят к периоцитам – отросчатым клеткам соединительной ткани, входящим в состав мелких сосудов и капилляров. Предшественниками периоцитов являются адвентициальные клетки – малодифференцированные клетки фибробластического ряда, сопровождающие кровеносные сосуды (рис. 2).
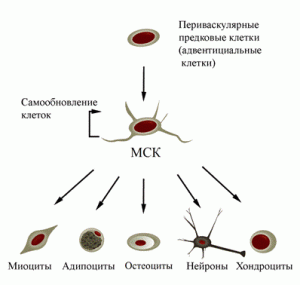 Рис. 2. Схема происхождения МСК. Возможные направления дифференцировки не выходят за пределы их зародышевого листка [7].
Рис. 2. Схема происхождения МСК. Возможные направления дифференцировки не выходят за пределы их зародышевого листка [7].
Международное общество по клеточной терапии (The International Society for Cellular Therapy) в 2006 г. утвердило три минимальных требования, позволяющих отнести стволовые клетки к МСК [8]:
1) адгезивность к пластику клеточных культур при культивировании в стандартных условиях;
2) экспрессия специфических поверхностных антигенов, определяемых методом проточной цитофлюориметрии у 95 % клеточной популяции: CD105 (мембранный гликопротеин эндоглин), CD73 (экто-5'-нуклеотидаза, 5'-НТ) и CD90 (гликопротеин Thy-1). Одновременно необходимо подтвердить этим же способом отсутствие экспрессии следующих поверхностных маркеров: CD45 (общий маркер для лейкоцитов), CD34 (маркер примитивных гематопоэтических клеток-предшественников и эндотелиальных клеток), CD14 или CD11b (экспрессируются на моноцитах и макрофагах, свидетельствуют о наличии гематопоэтических клеток в культуре МСК), CD79альфа или CD19 (маркеры B-клеток, которые могут в культуре клеток связываться с МСК путем адгезионного взаимодействия) и HLA II (молекулы HLA-DR не экспрессируются на поверхности МСК без стимуляции, например, IFN-гамма). Обнаружение экспрессии HLA-DR подтверждает, что клетки являются стимулированными МСК («stimulated MSC»);
3) наличие у клеток потенциала дифференцировки, т.е. они должны обладать способностью в условиях in vitro дифференцироваться в остеоциты, адипоциты и хондроциты. Дифференцировка в остеоциты демонстрируется окрашиванием ализариновым красным (alizarin red) или окрашиванием по фон Косса (von Kossa staining); дифференцировка в адипоциты – окрашиванием с красителем Oil Red O (Oil Red O staining); дифференцировка в хондроциты доказывается окрашивание альциановым синим (Alcian blue) или иммуногистохимическим окрашиванием на коллаген второго типа (collagen type II). Существуют и другие методы гистохимического окрашивания, подтверждающие потенциал дифференцировки стволовых клеток.
Фирма-производитель БМКП должна подтвердить соответствие БМКП этим требованиям в материалах регистрационного досье.
Получение клеточной линии определенного клеточного состава включает пять последовательно выполняемых этапов [3]. Заявителю необходимо также показать, что все указанные этапы выполнялись в помещениях, обеспечивающих асептические условия по классу А (табл. 1).
Таблица 1. Этапы получения клеточной линии определенного клеточного состава
|
Этап |
Действия разработчика БКМП |
Действия эксперта по оценке эффективности, безопасности и качества БМКП |
|
Отбор донора |
Отбор донора в соответствии с законами и подзаконными актами Российской Федерации; предоставление соответствующих документов в регистрационном досье |
Оценка соответствия процедуры отбора донора, изложенной в регистрационном досье, законам и подзаконным актам Российской Федерации |
|
Забор биологического материала |
Соблюдение условий проведения этапа (класс чистоты помещения не ниже А, сертифицированные методы отбора биологического материала, использование одноразовых инструментов); предоставление документов в регистрационном досье, подтверждающих последовательность действий и соответствие типа клеток клеткам ткани, являющейся источником их выделения |
Оценка соответствия процедуры отбора биологического материала, изложенной в регистрационном досье, требованиям нормативных документов; оценка документов регистрационного досье, подтверждающих последовательность действий на этапе и соответствие типа полученных клеток клеткам ткани, являющейся источником их выделения |
|
Выделение стволовых клеток из материала донора |
Соблюдение условий проведения этапа культивирования; предоставление документов в регистрационном досье, подтверждающих последовательность действий, правильности и стандартизации примененных методов (методик), соответствие полученных на этом этапе клеток клеткам ткани, являющейся источником их выделения |
Оценка документов регистрационного досье, подтверждающих соответствие методов выделения стволовых клеток, методам работы с данным типом стволовых клеток |
|
Получение стандартизуемой популяции однородных клеток |
Проведение серии последовательных пассажей для получения материала, пригодного для внесения в биореакторы (с целью получения БМКП); подтверждение степени однородности и зрелости популяции полученных на этом этапе клеток, их мезенхимальной природы; предоставление результатов в регистрационное досье |
Анализ приведенных доказательств степени однородности и зрелости популяции клеток, подтверждения их мезенхимальной природы |
|
Охарактеризование клеточного состава клеточной линии и ее паспортизация |
Необходимо подтвердить, что заявленная клеточная линия представляет собой линию МСК и может использоваться для терапевтических целей; предоставление результатов в регистрационное досье; паспортизация полученной клеточной линии |
Анализ приведенных доказательств степени однородности и зрелости популяции клеток, подтверждения их мезенхимальной природы, жизнеспособности, биохимической активности, целостности кариотипа, соответствия иммунофенотипическим маркерам клеточной дифференцировки и заявленному происхождению клеточной линии, потенциала дифференцировки; оценка результатов паспортизации полученной клеточной линии |
Первый этап получения клеточной линии определенного клеточного состава – «Отбор донора». Регулируется законодательными актами и подзаконными актами Российской Федерации. В проекте Федерального закона № 717040-6 от 06.02.2015 г. «О биомедицинских клеточных продуктах» [1] процедуре получения биологического материала для производства биомедицинского клеточного продукта посвящена глава 6. Порядок медицинского обследования донора биологического материала для выявления противопоказаний для получения биологического материала в целях производства биомедицинских клеточных продуктов, включая тестирование на носительство инфекционных агентов, и перечень противопоказаний (абсолютных и относительных) для получения биологического материала в целях производства биомедицинских клеточных продуктов будут утверждены уполномоченным федеральным органом исполнительной власти (см. п. 6 ст. 40 проекта Федерального закона № 717040-6 от 06.02.2015 г.) [1]. Задача эксперта на данном этапе – оценка по представленным документам соответствия использованной разработчиком БМКП процедуры отбора донора законодательным и подзаконным актам Российской Федерации.
Второй этап – «Забор биологического материала» предполагает осуществление в асептических условиях следующих операций:
- получение тканей донора (кожа, подкожно-жировая клетчатка, костный мозг, плацента, пульпа зуба и др.) специальными хирургическими инструментами;
- их измельчение (расслоение) с помощью мягкого механического воздействия (кожа, плацента, пуповина), разделения центрифугированием в градиенте фиколл-урографина (костный мозг) или дифференциальным осаждением (жировая ткань);
- получение из тканей донора смешанной суспезии клеток, обычно путем инкубирования в 0,1% растворе коллагеназы первого типа (кожа, ткань плаценты или пуповины);
- концентрирование дифференциальным осаждением (центрифугирование при 300 g) либо разделением в градиенте фиколл-урографина (для получения МСК костного мозга).
МСК из различных тканей одного вида неэквивалентны даже при том, что они сходны по основным иммунотипическим характеристикам [9]. Например, они могут иметь различия по способности к пролиферации и дифференцировке и по экспрессии некоторых маркеров. Установлено, что при одинаковом иммунофе`нотипе МСК из селезенки фетального происхождения имеют сниженные потенции к адипогенезу, а МСК из печени фетального происхождения – к остеогенезу [10]. МСК кожи дифференцируются только в адипоциты и, несмотря на свою мезенхимальную природу, они не обладают мультипотентностью, являясь, скорее, унипотентными клетками [11]. Поэтому эксперт при анализе материалов регистрационного досье, с привлечением научной литературы, должен сравнить соответствие типа клеток, указанных в спецификации на БМКП, клеткам ткани, являвшейся источником их выделения и медицинскому назначению БМКП.
Третий этап – «Выделение стволовых клеток из материалов донора». В полученной на предыдущем этапе суспензии клеток стволовые клетки составляют сотые доли процента. Морфологическая гетерогенность клеток суспензии вызвана наличием в ней клеток других тканей и различной степенью «зрелости» мезенхимальных клеток. Их относительное количество определяется особенностями ткани, из которой проводилось выделение клеток, и способом, использованным для получения клеточной суспензии.
Для выделения стволовых клеток из суспензии клеток используется такая особенность клеток мезенхимального происхождения, как адгезия к пластику [8]. Клеточную суспензию рассевают в концентрации 104 кл/мл в ростовой среде в культуральные флаконы с площадью поверхности 75 см2 и культивируют в стандартных условиях в СО2-инкубаторе (37? С, 5 % СО2, влажность 80 %) до достижения монослоем 80 %-ой конфлюэнтности со сменой ростовой среды каждые 3-е сут. В состав ростовой среды входит фактор роста фибробластов (бета-FGF). Типовой состав такой среды следующий: DMEM-F12; 10 % фетальная телячья сыворотка (для получения МСК для медицинских целей, использоваться не должна), не должна; 100 Ед./мл пенициллина; 100 Ед./мл стрептомицина; 2 мМ глютамин; 1 мМ пируват натрия; 10 нг/мл бета-FGF [11].
На этом этапе получить клеточную линию определенного клеточного состава обычно не удается из-за примеси клеток другого происхождения, способных к адгезии к пластику. Так, для клеточной суспензии, полученной из костного мозга, характерно наличие нескольких популяций клеток, способных прикрепляться к поверхности пластика. Для клеток, полученных из пуповины и плаценты, характерно наличие мезинхимальных клеток различной степени «зрелости». В ходе культивирования происходит постепенное увеличение доли мелких, митотически активных фибробластоподобных клеток (рис. 3 и 4).
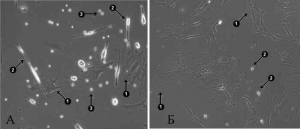 Рис. 3. Морфологически гетерогенная первичная культура (0 пассаж, 5 сут культивирования) МСК из плаценты (А) и пуповины (Б) человека. 1 – «распластанные» мезенхимальные клетки, переживающие адаптационный период; 2 – клетки крови, обладающие способностью прикрепляться к пластику; 3 – эритроциты. Увеличение 100 [11].
Рис. 3. Морфологически гетерогенная первичная культура (0 пассаж, 5 сут культивирования) МСК из плаценты (А) и пуповины (Б) человека. 1 – «распластанные» мезенхимальные клетки, переживающие адаптационный период; 2 – клетки крови, обладающие способностью прикрепляться к пластику; 3 – эритроциты. Увеличение 100 [11].
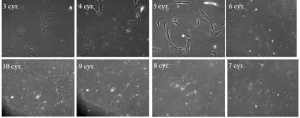 Рис. 4. Формирование монослоя первичной культурой МСК из пуповины человека (0 пассаж, 3–10 сут культивирования). Съемка проводилась на одном и том же участке культурального флакона при одинаковом увеличении ежесуточно. Смена среды проводилась каждые 3 сут. Показано постепенное увеличение доли мелких, митотически активных фибробластоподобных клеток в процессе культивирования. Увеличение 100 [11].
Рис. 4. Формирование монослоя первичной культурой МСК из пуповины человека (0 пассаж, 3–10 сут культивирования). Съемка проводилась на одном и том же участке культурального флакона при одинаковом увеличении ежесуточно. Смена среды проводилась каждые 3 сут. Показано постепенное увеличение доли мелких, митотически активных фибробластоподобных клеток в процессе культивирования. Увеличение 100 [11].
После образования мелких митотически активных фибробластоподобных клеток, их переводят в суспензию и рассевают в культуральные флаконы.
Четвертый этап – «Получение стандартизуемой популяции однородных клеток» предполагает наработку штокового клеточного материала, который в дальнейшем будет использован для выращивания клеток в биореакторах. По своей сути, этот процесс включает серию последовательных пассажей в стандартных условиях культивирования в ростовой среде, содержащей бета-FGF.
Обычно после второго пассажа клеточная культура выглядит морфологически гомогенной и содержит фибробластоподобные небольшие митотически активные веретенообразные клетки. Их метаболическая активность максимальна (период удвоения культуры – около 1 сут). Затем в культуре клеток происходит обратный процесс: после нескольких пересевов, приблизительно к V–VI пассажу, клетки постепенно теряют свою митотическую активность, в культуре снова появляются «распластанные» крупные клетки и рост клеток останавливается. Клетки в состарившейся культуре уже не подвержены дифференцировке. При помещении их в специальные дифференцировочные среды они не способны к дифференцировке ни по одному из направлений, характерных для МСК: остеогенному, хондрогенному или адипогенному. Митотически неактивные клетки, с низким уровнем пролиферации и метаболизма нельзя использовать для производства БМКП [11].
Пятый этап – «Охарактеризование клеточного состава клеточной линии и ее паспортизация». Разработчик БМКП должен получить и представить эксперту доказательства, что заявленная клеточная линия представляет собой линию МСК и может быть использована для терапевтических целей. Для этого он должен представить доказательства того, что [3]:
- иммунофенотип клеток соответствует характерному для МСК;
- линия клеток имеет происхождение, указанное в спецификации;
- клетки обладают потенциалом дифференцировки при неизмененных теломерах;
- клетки обладают выраженной биохимической активностью;
- линия клеток не содержат примесей ксеногенных клеточных линий;
- кариотип клеток клеточной линии стабилен;
- клетки жизнеспособны и количество живых клеток в линии превышает 90 %;
- в клеточной линии отсутствуют инфекционные агенты.
Минимальный иммунофенотип клеток, позволяющий отнести клетки, способные к адгезии к пластику, к мезенхимальным стволовым клеткам, приведен выше. У таких клеток возможна экспрессия и других маркеров клеточной адгезии: CD44, CD54, CD90 и CD106, играющих важную роль в процессе миграции и хоуминга, что характерно для клеток мезенхимального типа [12, 13]. Определение маркеров проводят с помощью проточной цитофлюорометрии.
Различия в экспрессии иммунофенотипических маркеров позволяют подтвердить соответствие клеточной линии тому, что указано в спецификации, т.е. ее подлинность (табл. 2).
Таблица 2. Особенности МСК в зависимости от источника выделения [14]
|
Особенность МСК |
Источник выделения МСК |
|||||
|
костный мозг |
пуповинная кровь |
ткань пуповины |
жировая ткань |
пульпа зуба |
плацента |
|
|
По способу выделения клеток |
Разделение в градиенте фикола-урографина |
Ферментативное или механическое разделение клеток, дифференциальное осаждение |
Ферментативное или механическое разделение клеток |
Ферментативное или механическое разделение клеток |
Вскрытие зуба, извлечение пульпы и ферментативная диссоциация ткани |
Мембранная сепарация. Вскрытие ткани плаценты, ферментативное или механическое разделение клеток, дифференциальное осаждение |
|
По иммунофенотипическим маркерам |
CD105, CD73 и CD90, CD45, CD34, CD14 или CD11b, CD79a или CD19 и HLA II |
Маркеры МСК костного мозга + Oct4, Nanog, Sox-2 (низкий уровень экспрессии) |
Маркеры МСК костного мозга + высокий уровень экспрессии CD146 |
Маркеры МСК костного мозга + высокий уровень экспрессии CD146; STRO-1 (негативен) |
Маркеры МСК костного мозга + STRO-1, CD146 |
Маркеры МСК костного мозга +SSEA-1, SSEA-4, Oct4, Nanog; более высокий уровень экспрессии CD49d, CD10 и CD56, чем у МСК костного мозга |
|
По ограничениям в клиническом применении |
Трудность при получении клеточной линии |
Низкий выход МСК |
МСК пуповины плохо изучены |
Гетерогенность популяции МСК |
Низкий выход МСК, их малая изученность |
Сложная процедура выделения МСК |
Экспрессия генов антигенов HLA-ABC не свидетельствует о том, что клеточная линия не относится к мезенхимальному типу, но делает ее пригодной только для аутологичных трансплантаций [11].
Потенциал дифференцировки линии МСК определяют по способности сформировавших ее клеток формировать остеоциты, адипоциты и хондроциты. Для этого используют специальные среды культивирования.
Клетки снимают с подложки культурального флакона в экспоненциальной фазе роста культуры с конфлюэнтностью 60–80 % по стандартной процедуре с трипсином/версеном (1:1) и рассевают в 24-луночные культуральные планшеты с покровными стеклами на дне лунок с начальной концентрацией 105 кл/лунка. Культивируют на протяжение 3 недель с заменой среды каждые 3 сут по стандартной методике в специальной среде. Для остеогенной дифференцировки используется среда следующего состава: DMEM-F12, 0,1 мкМ дексаметазон, 0,05 мМ аскорбиновая кислота, 10 мМ глицерофосфат кальция. Адипогенную дифференцировку оценивают путем выращивания клеток в среде DMEM-F12, содержащей 0,1 мкМ дексаметазон, 0,05 мМ аскорбиновая кислота, 10 нг/мл трансформирующего ростового фактора бета (TGF-β). Адипогенную дифференцировку МСК выполняют в среде DMEM-F12, 10% FBS, 1 мкМ дексаметазон, 0,5 мкМ изометилбутилксантин (IBMX), 100 мкМ индометацин, 10 мкг/мл инсулин. Подробно среды культивирования, включающие компоненты, способные управлять дифференцировкой стволовых клеток, и механизмы дифференцировки описаны в работе С. Vater и др. [15]. Дифференцировку клеток подтверждают стандартными иммуноцитохимическими методами [11, 16] (рис. 5).
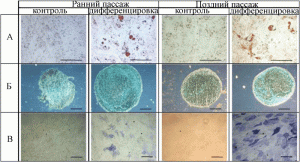 Рис. 5. Иммуноцитохимическое подтверждение дифференцировки МСК разных пассажей, полученных из ткани пуповины человека. А – дифференцировка МСК в адипоциты. Показана окрашиванием Oil Red O: вакуоли клетки, богатые липидами, имеют красный цвет (полоса соответствует 100 мкм). Б – дифференцировка МСК в хондроциты. Показана окрашиванием альциановым синим: глюкозаминогликаны и мукополисахариды окрашены в ярко-синий цвет. В – дифференцировка МСК в остеоциты. Показана окрашиванием щелочной фосфатазы – темно-синие структуры (полоса соответствует 200 мкм) [16].
Рис. 5. Иммуноцитохимическое подтверждение дифференцировки МСК разных пассажей, полученных из ткани пуповины человека. А – дифференцировка МСК в адипоциты. Показана окрашиванием Oil Red O: вакуоли клетки, богатые липидами, имеют красный цвет (полоса соответствует 100 мкм). Б – дифференцировка МСК в хондроциты. Показана окрашиванием альциановым синим: глюкозаминогликаны и мукополисахариды окрашены в ярко-синий цвет. В – дифференцировка МСК в остеоциты. Показана окрашиванием щелочной фосфатазы – темно-синие структуры (полоса соответствует 200 мкм) [16].
Биохимическую активность клеточной линии МСК и количество жизнеспособных клеток оценивают по ее суммарной дегидрогеназной активности с помощью МТТ-метода. Оптический сигнал в МТТ-методе прямо пропорционален количеству жизнеспособных клеток мезенхимального происхождения. Метаболический потенциал культуры меняется с возрастом клеток и количеством пассажей. После выделения клеток мезенхимального происхождения в культуру in vitro, дегидрогеназная активность возрастает на протяжении нескольких первых пассажей, но после пятого пассажа начинает постепенно снижаться. Этот эффект объясняется тем, что сразу после выделения клеточная культура обогащена зрелыми фибробластами, имеющими пониженный уровень метаболизма. Доля юных, метаболически активных клеток с каждым пассажем возрастает вследствие вытеснения ими из культуры зрелых клеток. Однако этот процесс не может продолжаться неограниченно долго, и постепенно доля метаболически активных клеток сокращается. Снижение доли метаболически активных клеток приводит к снижению дегидрогеназной активности, что регистрируется с помощью МТТ-метода [11]. Одновременно меняется морфология клеток, усиливается экспрессия бета-галактозидазы (маркер клеточного старения на моделях in vitro), экспрессия теломеразной обратной транскриптазы (human telomerase reverse transcriptase, hTERT) перестает определяться, теломеры хромосом укорачиваются [16–18] (рис. 6 и 7).
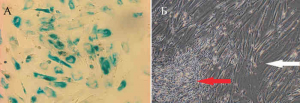 Рис. 6. Морфологические особенности клеток «состарившейся линии». А – бета-галактозидазная активность МСК поздних пассажей, полученных из пуповины человека. Бета-галактозидаза вызывает гидролиз X-gal, при этом образуется галактоза и 5-бромо-4-хлоро-3-гидроксииндол. Последний окисляется в 5,5'-дибромо-4,4'-дихлоро-индиго, образуя нерастворимый окрашенный в синий цвет продукт. Б – морфология МСК поздних пассажей, полученных из пуповины человека. Хорошо различимы быстро делящиеся маленькие фибробластные клетки (красная стрелка) и крупные распластанные по поверхности пластика клетки (белая стрелка), утратившие способность к делению [18].
Рис. 6. Морфологические особенности клеток «состарившейся линии». А – бета-галактозидазная активность МСК поздних пассажей, полученных из пуповины человека. Бета-галактозидаза вызывает гидролиз X-gal, при этом образуется галактоза и 5-бромо-4-хлоро-3-гидроксииндол. Последний окисляется в 5,5'-дибромо-4,4'-дихлоро-индиго, образуя нерастворимый окрашенный в синий цвет продукт. Б – морфология МСК поздних пассажей, полученных из пуповины человека. Хорошо различимы быстро делящиеся маленькие фибробластные клетки (красная стрелка) и крупные распластанные по поверхности пластика клетки (белая стрелка), утратившие способность к делению [18].
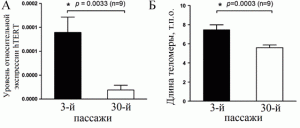 Рис. 7. Результаты анализа активности hTERT и размеров теломер ранних и поздних пассажей МСК, полученных из пуповины человека. А – уровень экспрессии hTERT. Б – уменьшение длины теломер с увеличение количества пассажей. В эксперименте использовалось 9 пар клонов МСК, полученных из пуповины человека. Дисфункция теломер, вызванная их укорачиванием, приводит к нестабильности кариотипа клетки, ее преждевременному старению или апоптозу [18].
Рис. 7. Результаты анализа активности hTERT и размеров теломер ранних и поздних пассажей МСК, полученных из пуповины человека. А – уровень экспрессии hTERT. Б – уменьшение длины теломер с увеличение количества пассажей. В эксперименте использовалось 9 пар клонов МСК, полученных из пуповины человека. Дисфункция теломер, вызванная их укорачиванием, приводит к нестабильности кариотипа клетки, ее преждевременному старению или апоптозу [18].
Оба процесса – старение клеток и их перерождение в злокачественные клетки, тесно связаны между собой. Поэтому укорочение теломер хромосом можно рассматривать как признак возможности злокачественно перерождения клетки уже после ее трансплантации реципиенту [3].
Для обнаружения ксеногенных клеточных линий целесообразно использовать гибридизацию in situ с ДНК близкородственных видов и клеток, обычно используемых в лабораториях. Сравнительные данные по экспрессии иммунофенотипических маркеров у разных видов животных противоречивы. Наиболее специфическим для линий клеток человека оказался рецептор CD13 – антитела к нему не давали перекрестной реакции с аналогичным рецептором МСК собак, свиней, коз, приматов, КРС и овец. Экспрессию рецепторов ксеногенных клеток могут подавлять МСК человека, например, рецептора CD271 [19]. Целесообразно проводить сравнение между отдельными хорошо охарактеризованными линиями клеток различного происхождения. Поэтому заявитель в материалах регистрационного досье должен указывать с линиями клеток каких видов животных он работал, и описать методы, позволяющие обнаружить примеси этих клеточных линий в БМКП.
Оценка стабильности кариотипа клеток является обязательным условием для трансплантации клеточной линии [20]. Анализ хромосомного состава клеток проводят путем цифровой обработки фотоизображений. Культуры МСК характеризуются малым количеством митозов. Чем более поздний пассаж, тем ниже митотическая активность клеточной популяции, тем менее активна ее теломераза, тем менее стабилен кариотип клетки (рис. 8).
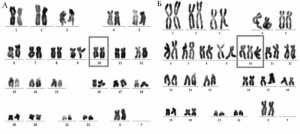 Рис. 8. Трисомия десятой хромосомы клона длительно пассируемых МСК, полученных из пуповины человека. А – нормальный кариотип. Б – трисомия десятой хромосомы [18].
Рис. 8. Трисомия десятой хромосомы клона длительно пассируемых МСК, полученных из пуповины человека. А – нормальный кариотип. Б – трисомия десятой хромосомы [18].
Способности клеточной линии вызывать у реципиента образование тератом изучают в опытах на иммунодефицитных самцах мышей линии C.B.-17/GbmsTac-scid-bgDF N7. Клетки имплантируют под капсулу яичек. Эмбриональные стволовые клетки линии H-9 используют в качестве положительного контроля. Рост тератомы определяют путем пальпации, мышей умерщвляют (обычно через 6,5–8,5 нед. после имплантации клеток) и опухолевую ткань исследуют гистологически [16].
Перечень инфекционных агентов, отсутствие которых в клеточной линии заявитель должен подтвердить в материалах регистрационного досье, будет утвержден уполномоченным федеральным органом исполнительной власти (п. 6 ст. 40 проекта Федерального закона № 717040-6 от 06.02.2015 г.) [1]. В него целесообразно включить возбудителей ВИЧ-инфекции (первого и второго типов), Т-клеточного лейкоза, сывороточных гепатитов, герпетических инфекций (вирусы герпеса 1 и 2 типов, цитомегаловирус). Заявитель должен подтвердить отсутствие контаминации клеточной линии бактериальными эндотоксинами, бактериями, микоплазмами, вирусами и простейшими.
Паспортизация является необходимой процедурой, документирующей результаты контроля состава, качества и безопасности клеточной линии. Паспортизация должна проводиться по результатам охарактеризования клеточной линии (табл. 3) и до проведения ее доклинических исследований. Общепринятой формы паспорта для клеточной линии нет. Общая структура паспорта, по мнению Буруновой [11], должна включать в себя четыре обязательных блока:
1) общая информация (научное название клеток; происхождение клеточного материала; маркировка образца; информация о доноре клеток);
2) жизнеспособность клеток (внешний вид образца; жизнеспособность клеток; стерильность; величина рН; цвет и консистенция образца; общая концентрация клеток, кл/мл; объем образца; время выдачи; срок годности, условия хранения);
3) результаты тестирования образца на отсутствие инфекционных агентов из списка, общего для всех типов клеток;
4) результаты тестирования образца на отсутствие инфекционных агентов, специфических для данного типа клеток.
Наработка клеток клеточной линии в количествах, позволяющих терапевтическое применение в составе БМКП
Процесс наработки клеточной линии в количествах, позволяющих их терапевтическое применение в составе БМКП, включает подбор питательной среды для выращивания МСК, культивирование в специальных биореакторах, контроль параметров культивирования.
Подбор питательной среды для выращивания МСК для терапевтического применения основывается на следующих принципах [3]:
питательная среда должна представлять собой «коктейль» из минеральных веществ, аминокислот, витаминов и не должна включать ксеногенные материалы, например, сыворотку эмбрионов крупного рогатого скота (fetal calf serum, FCS) или бычий сывороточный альбумин (bovine serum albumin, BSA), так как существует риск инфицирования культивируемых клеток возбудителями инфекционных болезней животных и последующей их передачи человеку;
в составе питательной среды должны быть факторы, ускоряющих рост МСК без изменения их дифференцировки. Например, добавление в среду ростового фактора тромбоцитов (platelet-derived growth factor, PDGF) и бета-FGF позволяет сократить цикл культивирования МСК с 4–6 нед. до 2–3 нед.;
все компоненты питательной среды должны иметь спецификацию. Наличие неохарактеризованных примесей биологически активных веществ, способно повлиять на дифференцировку клеток. Например, ростовой фактор тромбоцитов, полученный из лизатов тромбоцитов (platelet lysate, PL), сдвигает направление дифференцировки МСК костного мозга в сторону формирования остеобластов. Поэтому факторы роста должны быть получены генно-инженерным путем.
Процесс наработки клеток для получения БМКП включает следующие этапы:
внесение «посевного материала» в биореактор;
культивирование клеток в биореакторе;
сбор клеток и их подготовка к концентрированию;
концентрирование клеток;
фасовка клеток.
Для наработки клеток используют биореакторы. В качестве «посевного материала» в биореактор вносят культуру клеток, собранную на стадии логарифмического роста, предварительно трипсинизированную, после нейтрализации трипсина. Содержание клеток в посевном материале обычно составляет 1–3 млн/мл [21, 22].
Требования к биореакторам, используемым для производства клеточных линий, изложены в GMP (European GMP regulations, appendix 1) [3]. Производство клеточных линий должно осуществляться в асептических условиях, что предполагает использование закрытых автоматизированных систем культивирования клеток [2, 3, 22].
Оптимальных и универсальных биореакторов, предназначенных для получение клеточных линий, не существует. В таблице 3 приведены их основные характеристики.
Таблица 3. Основные характеристики биореакторов, используемых для культивирования МСК [2]
|
Тип биореактора |
Легкость сбора клеток |
Легкость мониторинга процесса культивирования |
Легкость масштабирования производства |
Массо-перенос |
Площадь поверхности культуры клеток (см2/л) |
Выход клеток (кл*106/мл) |
Стандартное окружение среды |
|
|
3D
|
2D
|
|||||||
|
«Статичная культура» |
Высокая |
Низкая |
Низкая |
Низкий |
290 |
0,1 |
Нет |
Да |
|
Волновой биореактор |
Высокая |
Средняя |
Высокая |
Средний |
Не определялась |
10–20 |
Нет |
Да |
|
Биореактор со встряхиванием среды (или в суспензии) |
Высокая |
Высокая |
Высокая |
Высокий |
2800 |
1–10 |
Да |
Да |
|
Эрлифт (перемешивание газовой фазой) |
Средняя |
Высокая |
Средняя |
Высокий |
2800 |
0,5 |
Да |
Да |
|
Биореактор с фильтрующим наполнителем |
Средняя |
Низкая |
Высокая |
Средний |
18 000 |
1,5–200 |
Да |
Да |
|
Биореактор с псевдоожиженным слоем |
Средняя |
Низкая |
Высокая |
Средняя |
25 000–75 000 |
5–100 |
Да |
Да |
|
Перфузионная камера (Aastrom Replicell) |
Средняя |
Средняя |
Средняя |
Средняя |
18 000 |
10–100 |
Нет |
Да |
|
Желобковый биореактор |
Средняя |
Средняя |
Средняя |
Средняя |
18 000–20 000 |
10–100 |
Нет |
Да |
|
Биореактор с системой полых волокон |
Низкая |
Низкая |
Средняя |
Средняя |
100 000–200 000 |
100–200 |
Нет |
Да |
|
Ротационный биореактор (Syntbecon) |
Средняя |
Средняя |
Низкая |
Средняя |
18 000–22000 |
Нет данных |
Нет |
Да |
Биореактор типа «статичная культура» (табл. 3) представляет собой обыкновенную колбу. В связи с невозможностью масштабирования процесса культивирования такой биореактор применяется только для лабораторных исследований или наращивания культуры клеток для аутологичной трансплантации. К его недостаткам можно отнести невозможность контроля процесса культивирования клеток по параметрам культуральной среды (физико-химические и др. параметры среды; см. ниже), а также ограниченность такого параметра технологического процесса, как «массоперенос» (скорость потребления клетками питательного субстрата из питательной среды). К достоинствам данного типа биореактора можно отнести его низкую себестоимость и простоту использования.
Волновой биореактор (табл. 3) по сути является полупроницаемым мешком, внутри которого находится культуральная жидкость. В отличие от биореактора типа «статичная культура», волновой биореактор позволяет проводить масштабирование процесса культивирования, но в ограниченных пределах. Процесс культивирования в таком биореакторе невозможно контролировать по параметрам культуральной среды. Поэтому он используется для получения клеточных линий для лабораторных экспериментов и аутологичной трансплантации.
В первом поколении биореакторов для масштабированного производства МСК использовали мультислойные системы, такие как CellStacks (Corning, Corning, NY, USA) или Cellfactory (Nunc, part of Thermo Fisher Scientific Inc., Waltham, MA, USA), помещаемые в инкубаторы (рис. 9).
 Рис. 9. Мультислойная система культивирования Cellfactory. 1 – ярусы для культивирования; 2 – вход и выход культуральной среды [23].
Рис. 9. Мультислойная система культивирования Cellfactory. 1 – ярусы для культивирования; 2 – вход и выход культуральной среды [23].
Биореакторы типа Cellfactory – модификация биореактора типа «статичная культура». Они имеют «развернутую» поверхность для культивирования и позволяют получать от нескольких сотен миллионов клеток до миллиарда в течение 2–3 нед. [24]. Однако согласно требованиям GMP, конструкция таких биореакторов не относится к полностью закрытым и для осуществления процесса культивирования их необходимо устанавливать в помещениях класса А, т.е. помещениях, обеспечивающих асептические условия процесса культивирования (табл. 4).
Таблица 4. Классы чистоты производственных помещений [25]
|
Класс чистоты помещений или зон |
Максимально допустимое количество частиц в 1 м3 воздуха размером, мкм |
Максимально допустимое количество жизнеспособных микроорганизмов в 1 м3 воздуха |
|||
|
≥ 0,5 |
≥ 5 |
≥ 0,5 |
≥ 5 |
||
|
оснащенное состояние |
функционирующее состояние |
||||
|
1 (А) |
3 500 |
0 |
3 500 |
0 |
Менее 1 |
|
2 (В) |
3 500 |
0 |
350 000 |
2 000 |
10 |
|
3 (С) |
350 000 |
2 000 |
3 500 000 |
20 000 |
100 |
|
4 (D) |
3 500 000 |
20 000 |
не определено |
200–500 |
|
|
* Требования и нормы зависят от вида готового продукта и характера выполняемых операций |
|||||
Остальные типы биореакторов, представленные в таблице 3, относятся к системам культивирования в объеме среды. Они позволяют осуществлять масштабирование технологического процесса и контролировать параметры культуральной среды. Получению в таких биореакторах клеточных линий, соответствующих показателям качества, способствует то обстоятельство, что при культивировании возможны взаимодействия по типу «клетка-клетка», «клетка-ростовой фактор» и «клетка-матрица». Эффективность массопереноса при культивировании клеток в объеме среды по сравнению с культивированием на плоскости увеличивается, культура клеток лучше обеспечена питательными субстратами, эффективнее взаимодействует с ростовыми факторами, при этом осуществляется отвод метаболитов от клеток. Данные системы культивирования предполагают практически одинаковый выход клеточного продукта – до 1?108 кл/мл. Однако и они имеют свои недостатки.
При использовании биореактора с механическим перемешиванием среды (встряхивание) клетки в процессе культивирования подвергаются физическому воздействию, которое может вызывать их повреждение еще до стадии выделения и концентрирования.
Биореактор типа «Эрлифт» имеет существенные ограничения по вязкости и плотности культуральной жидкости. В вязких плотных средах перемешивание газовой фазой (барботирование газа через слой культуральной среды) происходит неравномерно, при этом схлопывание пузырьков газа может оказывать травмирующее или разрушающее действие на растущие клетки. В биореакторах данного типа происходит обильное пенообразование, что не позволяет использовать весь объем аппарата, а применение химического пеногасителя сказывается на качестве конечного продукта.
Наиболее эффективным типом биореактора для культивирования МСК, по мнению Placzek et al. [2], является биореактор с системой полых волокон (рис. 10).
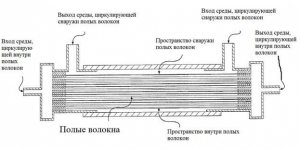 Рис. 10. Схема биореактора на полых волокнах. Циркулирование питательной среды предполагается внутри полых волокон, клетки располагаются снаружи полых волокон [22].
Рис. 10. Схема биореактора на полых волокнах. Циркулирование питательной среды предполагается внутри полых волокон, клетки располагаются снаружи полых волокон [22].
Полые волокна представляют собой полупроницаемую мембрану из растяжимого материала, на поверхности которого возможна фиксация клеток, например, как показано на рисунке 11 [23].
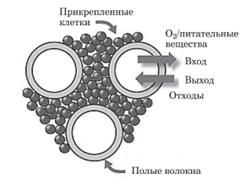 Рис. 11. Схема расположения клеток в реакторе на полых волокнах [23].
Рис. 11. Схема расположения клеток в реакторе на полых волокнах [23].
Преимущество биореакторов на полых волокнах перед биореакторами других типов заключается в щадящем режиме культивирования. Для данного типа биореакторов существует ограничение по рабочему объему (120–150 см3) [23].
Для повышения безопасности клеточного продукта и упрощения процесса его производства должны использоваться биореакторы, изготовленные из стандартных одноразовых модулей, имеющие большое соотношение поверхности для культивирования клеток к объему реактора, закрытую систему культивирования, автоматизированные процессы выполнения инокуляции посевного материала и сбора клеток, автоматизированный постоянный контроль параметров культивирования с помощью одноразовых датчиков [22, 26, 27].
Использование закрытых автоматизированных систем культивирования клеток позволяет осуществлять процесс получения клеточных линий в производственных помещениях класса чистоты C или D [3].
Получение клеточных линий необходимого качества требует тщательного контроля процесса культивирования. Постоянному контролю подлежат [2]:
физико-химические параметры среды (стандартные физико-химические параметры культивирования клеток: pH 7,4; О2 – 20%; СО2 – 5%; температура 37 0С);
содержание в среде питательных компонентов и метаболитов;
содержание в среде ростовых факторов.
Сбор клеток и их подготовка к концентрированию осуществляются путем декантации или отбора другим способом среды, содержащей клетки. Способ отбора зависит от типа биореактора. Далее к клеточной суспензии добавляют трипсин (с ЭДТА) до 0,25% и инкубируют при температуре 370С в течение 3–5 мин, трипсин нейтрализуют, суспензию клеток собирают в специальной емкости для последующего концентрирования и фасовки во флаконы.
Концентрирование клеток осуществляется с помощью щадящих технологий (например, тангенциальной фильтрацией) в полностью автоматизированном режиме [21].
Один из вариантов автоматизированного осуществления процесса асептического выделения и концентрирования МСК из культуральной среды предложен американской фирмой Lonza Walkersville, Inc (рис. 12).
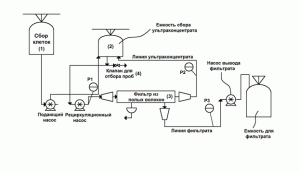 Рис. 12. Схема процесса выделения и концентрирования клеток в тангенциальном потоке [28, 29].
Рис. 12. Схема процесса выделения и концентрирования клеток в тангенциальном потоке [28, 29].
Технологически процесс концентрирования клеточной массы после стадии культивирования можно условно разделить на три этапа. Первый этап – асептический перенос клеточной массы в специальную емкость сбора (1), которую подключают к системе ультрафильтрации. Второй этап – перекачивание клеточной массы из емкости сбора клеток в рабочую емкость (2). После завершения перекачивания емкость сбора и подающий насос отключаются от системы ультрафильтрации. Из рабочей емкости клеточная масса с помощью рециркулирующего насоса начинает медленно подаваться на мембранный фильтр (3) с размером пор 0,5–0,65 мкм, состоящий из полых волокон, с последующим увеличением скорости подачи клеточной массы на фильтр. Прокачка жидкости осуществляется перистальтическими насосами. После достижения оптимальной скорости подачи клеточной массы от 50 до 300 л/м2?ч включается насос вывода фильтрата. Фильтрация осуществляется при невысоком давлении (1 psi или 6894,76 Па). При необходимости цикл концентрирования повторяют. Датчики Р1, Р2, Р3, задействованные в процессе концентрирования (см. рис. 12), являются одноразовыми. В процессе концентрирования, используя клапан для отбора проб (4), периодически извлекают пробу клеточной массы для оценки клеточной плотности и жизнеспособности клеток. Данная система позволяет получать концентрат биомассы с содержанием 10–200 млн жизнеспособных кл/мл. Одним из преимуществ данной технологической схемы является сохранение жизнеспособными в концентрате не менее 70–90% клеток.
Фасовка во флаконы осуществляется с использованием автоматизированных линий, обеспечивающих асептические условия всего процесса [21].
Контроль качества и стандартизация полученной клеточной линии
Проект Федерального закона № 717040-6 от 06.02.2015 г. «О биомедицинских клеточных продуктах» [1] определяет качество биомедицинского клеточного продукта как соответствие биомедицинского клеточного продукта требованиям нормативной документации. Проведенный нами ранее анализ структуры патентования фирмами, ведущими в области разработки препаратов на основе клеточных технологий [30], позволяет предположить, что разработка таких требований будет идти по двум направлениям – общие требования к показателям качества, применимые ко всем клеточным линиям, и частные, которые будут использоваться для оценки терапевтических препаратов, имеющих свой круг показаний (например, для лечения сахарного диабета, костной пластики, восстановление кровоснабжения ишемизированного миокарда).
К общим требованиям к качеству клеточных линий, включаемых в БМКП, и которые заявитель должен подтверждать материалами регистрационного досье, Sensebe et al. [3], Placzek et al. [2], Бурунова [11] и Kolkundkar et al. [21] относят следующие:
иммунофенотип клеток должен соответствовать заявленному происхождению клеточной линии и стадии их дифференцировки;
результаты гистохимического исследования должны подтверждать потенциал дифференцировки клеточной линии;
данные МТТ-анализа должны подтверждать жизнеспособность клеток клеточной линии и соответствие количества живых клеток требованиям нормативной документации;
уровень экспрессии теломеразной обратной транскриптазы и длина теломер не должны быть меньшими, чем у клеток нулевого пассажа;
данные кариотипирования должны подтверждать стабильность кариотипа клеток;
данные по иммуногенности клеток должны подтверждать отсутствие иммуномодулирующего или иммуносупрессивного эффекта после их введения реципиенту (если такой эффект не является целью разработки препарата);
должны быть приведены доказательства отсутствия в БМКП клеток ксеногенных клеточных линий;
должны быть приведены данные, доказывающие отсутствие контаминации клеточной линии бактериальными эндотоксинами, бактериями, микоплазмами, вирусами и простейшими, и способности клеток вызывать образование тератом;
если клеточная линия предназначена для аллогенного или комбинированного БМКП, то должны быть приведены доказательства ее карантинизации. С учетом максимальной продолжительности латентного периода гемотрансмиссивных инфекций, карантинизация клеточной линии должна быть продолжительностью не менее 180 сут., как это делается при использовании свежезамороженной плазмы [31]. При выявлении в период карантинизации вирусоносительства или заболевания донора (ВИЧ, вирусные гепатиты) вся заготовленная от него клеточная линия бракуется.
Частные требования в данной работе не рассматриваются из-за большого разнообразия направлений создания таких БМКП.
Исследование выполнено при финансовой поддержке Министерства образования и науки (проект RFMEFI61014X0001).
Литература:
1. О биомедицинских клеточных продуктах. Проект Федерального закона № 717040-6 от 06.02.2015 г. [cited 2015 March 5]. Available from: http://asozd2.duma.gov.ru/main.nsf/%28SpravkaNew%29?OpenAgent&RN=717040-6&02.
2. Placzek MR, Chung I-M, Macedo HM, Ismail S, Blanco TM, Lim M et al. Stem cell bioprocessing: fundamentals and principles. J. R. Soc. Interface 2009; 6: 209–32.
3. Sensebe L, Gadelorge M, Fleury-Cappellesso S. Production of mesenchymal stromal/stem cells according to good manufacturing practices: a review. Stem Cell Res. Therapy 2013; 4: 66–71.
4. Liras A. Future research and therapeutic applications of human stem cells: general, regulatory, and bioethical aspects. J. Transl. Med. 2010; 8: 131.
5. Rigotti G, Marchi A, Sbarbati A. Adipose-derived mesenchymal stem cells: past, present, and future. Aesthet Plast Surg. 2009; 33: 271–3.
6. Lombardo E, van der Poll T, DelaRosa O, Dalemans W. Mesenchymal stem cells as a therapeutic tool to treat sepsis. World J Stem Cells 2015; 7(2): 368–79.
7. Adipogenic differentiation and analysis of MSC. PromoCell GmbH. [cited 2015 March 5]. Available from: www.promocell.com.
8. Dominici M, Le Blanc K, Mueller I, Slaper-Cortenbach I, Marini F, Krause D, et al. Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement. Cytotherapy 2006; 8: 315–7.
9. Phinney DG, Sensebe L. Mesenchymal stromal cells: misconceptions and evolving concepts. Cytotherapy 2013; 15: 140–5.
10. Pieternella S, Noort WA, Scherjon SA, Kleuburg-van der Keur G, Krusselbrink AB, van Bezoouen RL, et al. Mesenchymal stem cells in human second-trimester bone marrow, liver, lung, and spleen exhibit a similar immunophenotype but a heterogeneous multilineage differentiation potential. J Hematol. 2003; 88: 845–52.
11. Бурунова ВИ. Проблемы стандартизации при получении клеточных культур мезенхимального происхождения: экспериментальный и теоретический анализ: автореф. дис. … канд. биол. наук. М.; 2011.
12. Goodwin HS, Bicknese AR, Chien SN, Bogucki BD, Quinn CO, Wall DA. Multilineage differentiation activity by cells isolated from umbilical cord blood: expression of bone, fat, and neural markers. Biol Blood Marrow Transplant. 2001; 7(11): 581–8.
13. Gronthos S, Franklin DM, Leddy HA, Robey PG, Storms RW, Gimble JM. Surface protein characterization of human adipose tissue-derived stromal cells. J Cell Physiol. 2001; 189(1): 54–63.
14. Viswanathan S, Keating A, Deans R, Hematti P, Prockop D, Stroncek DF, et al. Soliciting strategies for developing cell-based reference materials to advance mesenchymal stromal cell research and clinical translation. Stem Cells Develop. 2014; 23(11): 1157–67.
15. Vater C, Kasten P, Stiehler M. Culture media for the differentiation of mesenchymal stromal cells. Acta Biomaterialia 2011; 7: 463–77.
16. Martins JP, Santos JM, de Almeida JM, Filipe MA, de Almeida MV, Almeida SC, et al. Towards an advanced therapy medicinal product based on mesenchymal stromal cells isolated from the umbilical cord tissue: quality and safety data. Stem Cell Res Ther. 2014; 5(1): 9. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4055140/pdf/scrt398.pdf.
17. Giardini MA, Segatto M, da Silva MS, Nunes VS, Cano MI. Telomere and telomerase biology. Prog Mol Biol Transl Sci. 2014; 125: 1–40.
18. Wang Y, Zhang Z, Chi Y, Zhang Q, Xu F, Yang Z, et al. Long-term cultured mesenchymal stem cells frequently develop genomic mutations but do not undergo malignant transformation. Cell Death and Disease. 2013; 4: e950. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3877551/pdf/cddis2013480a.pdf.
19. Boxall SA, Jones E. Markers for characterization of bone marrow multipotential stromal cells. Stem Cells Intern. 2012; Article ID 975871. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3361338/pdf/SCI2012-975871.pdf.
20. Chase LG, Yang S, Zachar V, Yang Z, Lakshmipathy U, Bradford J et al. Development and characterization of a clinically compliant xeno-free culture medium in good manufacturing practice for human multipotent mesenchymal stem cells. Stem Cells Transl. Med. 2012; 1: 750–8.
21. Kolkundkar U, Gottipamula S, Majumdar AS. Cell therapy manufacturing and quality control: current process and regulatory challenges. J Stem Cell Res Ther. 2014; 4(9). Available from: http://omicsonline.org/open-access/cell-therapy-manufacturing-and-quality-control-current-process-and-regulatory-challenges-2157-7633.1000230.pdf.
22. Hirschel M, Wojciechowski RJ, Arneson K. Biomanufacturing suite and methods for large-scale production of cells, viruses, and biomolecules. App. WO № 2014/036187; 2014.
23. Чулкова ТЮ, Курбанова ЕК, Новиков ЮН, Гусаров ДА. Одноразовые системы. Плюсы и минусы использования. Решения для апстрим процесса (мини-обзор). Биофармацевтический журнал 2013; 5(1): 3–12.
24. Tarte K, Gaillard J, Lataillade JJ, Fouillard L, Becker M, Mossafa H, et al. Societe Francaise de Greffe de Moelle et Therapie Cellulaire: clinical-grade production of human mesenchymal stromal cells: occurrence of aneuploidy without transformation. Blood 2010; 115: 1549–53.
25. Надлежащая практика производства медицинских иммунобиологических препаратов. Санитарно-эпидемиологические правила СП 3.3.2.1288–03. М., 2003.
26. Godara P, McFarland CD, Nordon RE. Design of bioreactors for mesenchymal stem cell tissue engineering. J Chem Technol Biotechnol. 2010; 83: 408–20.
27. Шустер АМ, Ручко СВ, Щукин МВ, Александров ВН, Говоров ИВ, Григорьева ОВ. и др. Опыт создания промышленной линии для производства клеточных продуктов. Биопрепараты 2014; (4): 37–41.
28. Rowley J, Pattasseril J, Mohamed A. High yield method and apparatus for volume reduction and washing of therapeutic cells using tangential flow filtration. Pat. CA № 2787656; 2011.
29. Rowley J, Pattasseril J, Mohamed A. High yield method and apparatus for volume reduction and washing of therapeutic cells using tangential flow filtration. App. WO № 2011/091248; 2011.
30. Супотницкий МВ, Елапов АА, Борисевич ИВ, Климов ВИ, Лебединская ЕВ, Миронов АН, Меркулов ВА. Перспективные методические подходы к доклиническому исследованию биомедицинских клеточных продуктов и возможные показатели их качества. Биопрепараты 2015; (1): 36–44.
31. О внедрении в практику работы службы крови в Российской Федерации метода карантинизации свежезамороженной плазмы. Приказ Минздрава РФ от 07.05.2003 № 193 (ред. от 19.03.2010) [cited 2015 March 5]. Available from: http://www.transfusion.ru/2010/04-19-2.html.
References
1. On biomedical cell products. The draft Federal Law № 717040-6, 06.02.2015 [cited 2015 March 5]. Available from: http://asozd2.duma.gov.ru/main.nsf/%28SpravkaNew%29?OpenAgent&RN=717040-6&02 (in Russian).
2. Placzek MR, Chung I-M, Macedo HM, Ismail S, Blanco TM, Lim M et al. Stem cell bioprocessing: fundamentals and principles. J. R. Soc. Interface 2009; 6: 209–32.
3. Sensebe L, Gadelorge M, Fleury-Cappellesso S. Production of mesenchymal stromal/stem cells according to good manufacturing practices: a review. Stem Cell Res. Therapy 2013; 4: 66–71.
4. Liras A. Future research and therapeutic applications of human stem cells: general, regulatory, and bioethical aspects. J. Transl. Med. 2010; 8: 131.
5. Rigotti G, Marchi A, Sbarbati A. Adipose-derived mesenchymal stem cells: past, present, and future. Aesthet Plast Surg. 2009; 33: 271–3.
6. Lombardo E, van der Poll T, DelaRosa O, Dalemans W. Mesenchymal stem cells as a therapeutic tool to treat sepsis. World J Stem Cells 2015; 7(2): 368–79.
7. Adipogenic differentiation and analysis of MSC. PromoCell GmbH. [cited 2015 March 5]. Available from: www.promocell.com.
8. Dominici M, Le Blanc K, Mueller I, Slaper-Cortenbach I, Marini F, Krause D, et al. Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement. Cytotherapy 2006; 8: 315–7.
9. Phinney DG, Sensebe L. Mesenchymal stromal cells: misconceptions and evolving concepts. Cytotherapy 2013; 15: 140–5.
10. Pieternella S, Noort WA, Scherjon SA, Kleuburg-van der Keur G, Krusselbrink AB, van Bezoouen RL, et al. Mesenchymal stem cells in human second-trimester bone marrow, liver, lung, and spleen exhibit a similar immunophenotype but a heterogeneous multilineage differentiation potential. J Hematol. 2003; 88: 845–52.
11. Burunova VI. Problems of standardization in the preparation of cell cultures of mesenchymal origin: an experimental and theoretical analysis. Cand.Biol.Sci [thesis]. Moscow; 2011 (in Russian).
12. Goodwin HS, Bicknese AR, Chien SN, Bogucki BD, Quinn CO, Wall DA. Multilineage differentiation activity by cells isolated from umbilical cord blood: expression of bone, fat, and neural markers. Biol Blood Marrow Transplant. 2001; 7(11): 581–8.
13. Gronthos S, Franklin DM, Leddy HA, Robey PG, Storms RW, Gimble JM. Surface protein characterization of human adipose tissue-derived stromal cells. J Cell Physiol. 2001; 189(1): 54–63.
14. Viswanathan S, Keating A, Deans R, Hematti P, Prockop D, Stroncek DF, et al. Soliciting strategies for developing cell-based reference materials to advance mesenchymal stromal cell research and clinical translation. Stem Cells Develop. 2014; 23(11): 1157–67.
15. Vater C, Kasten P, Stiehler M. Culture media for the differentiation of mesenchymal stromal cells. Acta Biomaterialia 2011; 7: 463–77.
16. Martins JP, Santos JM, de Almeida JM, Filipe MA, de Almeida MV, Almeida SC, et al. Towards an advanced therapy medicinal product based on mesenchymal stromal cells isolated from the umbilical cord tissue: quality and safety data. Stem Cell Res Ther. 2014; 5(1): 9. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4055140/pdf/scrt398.pdf.
17. Giardini MA, Segatto M, da Silva MS, Nunes VS, Cano MI. Telomere and telomerase biology. Prog Mol Biol Transl Sci. 2014; 125: 1–40.
18. Wang Y, Zhang Z, Chi Y, Zhang Q, Xu F, Yang Z, et al. Long-term cultured mesenchymal stem cells frequently develop genomic mutations but do not undergo malignant transformation. Cell Death and Disease. 2013; 4: e950. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3877551/pdf/cddis2013480a.pdf.
19. Boxall SA, Jones E. Markers for characterization of bone marrow multipotential stromal cells. Stem Cells Intern. 2012; Article ID 975871. [cited 2015 March 25]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3361338/pdf/SCI2012-975871.pdf.
20. Chase LG, Yang S, Zachar V, Yang Z, Lakshmipathy U, Bradford J et al. Development and characterization of a clinically compliant xeno-free culture medium in good manufacturing practice for human multipotent mesenchymal stem cells. Stem Cells Transl. Med. 2012; 1: 750–8.
21. Kolkundkar U, Gottipamula S, Majumdar AS. Cell therapy manufacturing and quality control: current process and regulatory challenges. J Stem Cell Res Ther. 2014; 4(9). Available from: http://omicsonline.org/open-access/cell-therapy-manufacturing-and-quality-control-current-process-and-regulatory-challenges-2157-7633.1000230.pdf.
22. Hirschel M, Wojciechowski RJ, Arneson K. Biomanufacturing suite and methods for large-scale production of cells, viruses, and biomolecules. App. WO № 2014/036187; 2014.
23. Chulkova TYu, Kurbanova EK, Novikov YuN, Gusarov DA. Disposable system. Pros and cons of using. Solutions for upstream process (mini-review). Biofarmatsevticheskiy zhurnal 2013; 5(1): 3–12 (in Russian).
24. Tarte K, Gaillard J, Lataillade JJ, Fouillard L, Becker M, Mossafa H, et al. Societe Francaise de Greffe de Moelle et Therapie Cellulaire: clinical-grade production of human mesenchymal stromal cells: occurrence of aneuploidy without transformation. Blood 2010; 115: 1549–53.
25. Good Manufacturing Practices for medical immunobiological preparations. Sanitary rules SP 3.3.2.1288–03. Мoscow; 2003 (in Russian).
26. Godara P, McFarland CD, Nordon RE. Design of bioreactors for mesenchymal stem cell tissue engineering. J Chem Technol Biotechnol. 2010; 83: 408–20.
27. Shuster AM, Ruchko SV, Schukin MV, Aleksandrov VN, Govorov IV, Grigorieva OV, et al. Experience of creation of industrial lines for the production of cellular products. Biopreparaty 2014; (4): 37–41 (in Russian).
28. Rowley J, Pattasseril J, Mohamed A. High yield method and apparatus for volume reduction and washing of therapeutic cells using tangential flow filtration. Pat. CA № 2787656; 2011.
29. Rowley J, Pattasseril J, Mohamed A. High yield method and apparatus for volume reduction and washing of therapeutic cells using tangential flow filtration. App. WO № 2011/091248; 2011.
30. Supotnitskiy MV, Elapov AA, Borisevich IV, Klimov VI, Lebedinskaya EV, Mironov AN, Merkulov VA. Promising methodological approaches to preclinical studies of biomedical cell-based products and their possible quality characteristics. Biopreparaty 2015; (1): 36–44 (in Russian).
31. On the implementation in practice of the blood service in the Russian Federation method quarantine fresh frozen plasma. Order of the Ministry of Health of the Russian Federation from 07.05.2003 № 193 (ed. by 19.03.2010) [cited 2015 March 5]. Available from: http://www.transfusion.ru/2010/04-19-2.html (in Russian).
Библиографическое описание: Супотницкий МВ, Елапов АА, Меркулов ВА, Борисевич ИВ, Климов ВИ, Миронов АН. Основные технологические процессы, используемые при производстве биомедицинских клеточных продуктов. Биопрепараты 2015; (2): 36–45.
Bibliographic description: Supotnitskiy MV, Elapov AA, Merkulov VA, Borisevich IV, Klimov VI, Mironov AN. Common technological processes used in manufacture of biomedical cell culture products. Biopreparation (Biopharmaceuticals) 2015; (2): 36–45.

Михаил Васильевич Супотницкий
Российский микробиолог, полковник медицинской службы запаса, изобретатель, автор книг и статей по истории эпидемий чумы и других особо опасных инфекций, истории разработки и применения химического и биологического оружия. Заместитель главного редактора научно-практического журнала «Вестник войск РХБ защиты» Министерства обороны РФ.
Метки: 2015, биомедицинский клеточный продукт