Механизмы развития резистентности к антибиотикам у бактерий
Повсеместность распространения обоих явлений — способность отдельных микроорганизмов синтезировать антибиотики, других — обладать резистентностью к ним, обусловлена тем, что антибиотики в концентрациях, встречающихся в природных экосистемах, играют роль внутриклеточных сигнальных молекул, регулирующих транскрипцию генов. Изменение реакции бактериального коммуникативного сообщества на определенный сигнал, вызванное приобретением, или, наоборот, утратой антибиотикорезистентности, приводит к образованию новых экотопов. Поэтому проблема антибиотикорезистентности среди клинически значимых микроорганизмов уходит своими корнями в сложные экологические и эволюционные отношения между самими микроорганизмами, сложившиеся задолго до появления человека как биологического вида. В основе механизма распространения генов антибиотикорезистентности между бактериями лежит обмен плазмидами и конъюгативными транспозонами. В эволюции антибиотикорезистентности плазмиды и конъюгативные транспозоны выполняют функцию генетических платформ, на которых посредством рекомбинационных систем бактерий происходит сборка и сортировка генов антибиотикорезистентности, включенных в транспозоны, интегроны, генные кассеты и инсерционные криптические последовательности. К настоящему времени известно не менее четырех биохимических механизмов, отвечающих за развития у бактерий антибиотикорезистентности: детоксикация антибиотика; уменьшение проницаемости стенки микроорганизма для антибиотиков и/или выкачивание его из клетки; структурные изменения в молекулах, являющихся мишенями для антибиотиков; продукция альтернативных мишеней для антибиотиков. Высокие уровни антибиотикорезистентности у грамотрицательных бактерий обусловлены их способностью детоксицировать антибиотики в периплазматическом пространстве. В клеточной стенке грамположительных бактерий периплазматическое пространство отсутствует, поэтому механизмы их детоксикационной резистентности к антибиотикам менее эффективны, чем у грамотрицательных бактерий. Целесообразно расширить круг исследуемых проблем, связанных с распространением антибиотикорезистентных патогенных микроорганизмов в клинике, включив в него процессы накопления и обмена генов антибиотикорезистентности среди бактерий в природных экосистемах.
Супотницкий М.В. Механизмы развития резистентности к антибиотикам у бактерий // Биопрепараты. — 2011. — № 2. — С. 4–44.
An ubiquity of both phenomena – the ability of some microorganisms to synthesize antibiotics, and others – to have resistance to them, caused to the fact that antibiotics at concentrations detected in natural ecosystems, are revealed the intracellular signaling molecules regulating gene transcription. Change in the reaction of bacterial community on special signal, caused by acquirement or, conversely, deprivation of antibiotic resistance leads to the appearance of new ecotopes. Therefore the problem of antibiotic resistance among clinically important microorganisms is rooted in complicated ecological and evolutional relations between microorganisms, developed long before appearance human being as biological species. Exchange of plasmids and conjugative transposons underlies of antibiotic resistance gene expansion mechanism between bacteria. In the evolution of antibiotic resistance the plasmids and conjugative transposons act as genetic platforms, on which via recombination systems of bacteria proceed an assembly and sorting antibiotic resistance genes, are included in the transposons, integrons, gene cassettes and insertion cryptic sequences, proceed. It is known at this point at least four biochemical mechanisms responsible for the development of antibiotic resistance in bacteria: detoxification of antibiotic; permeability reduction of microorganism cell wall for antibiotics and/or deflation antibiotic from the cell; structural changes in molecules that are targets for antibiotics, production of alternative targets for antibiotics. High levels of antibiotic resistance in Gramnegative bacteria associated to their ability to detoxify antibiotics in periplasmatic space. There is not periplasmatic space in the cell wall of Gram-positive bacteria. Therefore, their mechanisms of detoxification antibiotic resistance are less effective than in Gram-negative bacteria. It is reasonable to extend the range of the problem being investigated, associated with the spread of antibiotic resistant pathogenic microorganisms in a clinic to include the processes of accumulation and exchange of antibiotic resistance genes among bacteria in the natural ecosystems.
Supotnitskiy М.V. Mechanisms of Antibiotics Resistance in Bacteria // Biopreparats (Biopharmaceuticals) — 2011. — No. 2. — P. 4–11.
Широкое применение антибиотиков в медицине и сельском хозяйстве сопровождается распространением антибиотикорезистентных патогенных микроорганизмов в клинике. За последнее десятилетие при помощи методов молекулярного анализа получены данные, значительно расширившие представления о механизмах появления и распространения генов антибиотикорезистентности среди микроорганизмов, имеющих клиническое значение. Целью настоящей работы является рассмотрение механизмов развития резистентности к антибиотикам у бактерий. Особое внимание уделяется определению роли в этом процессе мобильных генетических элементов, а также биохимическим различиям антибиотикорезистентности у грамположительных и грамотрицательных микроорганизмов.
Антибиотики как сигнальные молекулы. Бактерии в естественных условиях образуют коммуникативные сообщества, включающие представителей разных таксонов, в которых и между которыми обмен информацией осуществляется посредством так называемых диффундирующих сигнальных молекул (diffusible signal molecules). Это низкомолекулярные вещества, взаимодействующие с системой клеточных рецепторных структур (мишеней). К их числу относятся и антибиотики (анти- + греч. bios жизнь) — органические молекулы с молекулярной массой в пределах 3 тыс. Да, получившие такое название из-за их бактерицидного или бактериостатического действия в концентрациях, обычно не встречающихся в природных экосистемах. Бактерии используют диффундирующие сигнальные молекулы для: 1) мониторинга своей популяционной плотности (the process of quorum sensing); 2) защиты своей экологической ниши; 3) координации своего поведения в отношении каких-то изменившихся условий внешней среды; 4) «наблюдения» за другими коммуникативными сообществами [18]. Биосинтетические пути антибиотиков сформировались у микроорганизмов еще до образования многоклеточной жизни. Например, у актиномицетов биосинтетические пути эритромицина и стрептомицина существуют не менее чем 500 млн лет [5].
Количество клеточных мишеней для диффундирующих сигнальных молекул, огромно. Ими являются не только рецепторные белки на поверхности бактерий, но и макромолекулярные структуры цитоплазмы. Первичный механизм, контролирующий функции бактериальной клетки, — регуляция транскрипции отдельных генов. Например, любой из 50 рибосомальных белков или РНК, может быть специфическим рецептором, связывающим такие молекулы, как аминогликозиды и макролидные антибиотики. Экспериментально установлено, что субингибирующие концентрации антибиотиков либо увеличивают, либо, наоборот, уменьшают количество транскриптов в различных бактериальных клетках [13, 26]. Отдельные примеры взаимодействия антибиотиков с внутриклеточными рецепторами, перечислены в табл. 1.
Таблица 1. Примеры взаимодействия антибиотиков с внутриклеточными рецепторами*
|
Биохимический процесс |
Функциональный рецептор |
Мишень |
Антибиотик |
|
Трансляция (синтез полипептидной цепи рибосомой с использованием в качестве матрицы мРНК) |
Рибосомы |
30S-субъединица |
Стрептомицин, гентамицин |
|
Спектиномицин |
|||
|
Тетрациклин |
|||
|
59S-субъединица |
Хлорамфеникол |
||
|
Эритромицин |
|||
|
Виргиниамицин |
|||
|
Линкомицин |
|||
|
Рибосомо-связывающие факторы |
Фактор элонгации Tu |
Кирромицин (kirromycin) |
|
|
Рибосомо-ассоциированные факторы |
Изолейцил-тРНК-синтетаза
|
Мупироцин (mupirocin) |
|
|
Транскрипция (процесс синтеза РНК с использованием ДНК в качестве матрицы) |
РНК-полимераза |
Бета-субъединица |
Рифампицин |
|
Бета-субъединица и бета штрих-субъединица |
Стрептолидигин (streptolydigin) |
||
|
Бета штрих-субъединица |
Микроцин J25 |
||
|
Репликация (процесс синтеза комплементарных нитей ДНК по матричной молекуле ДНК) |
ДНК-гираза |
Субъединица А |
Новобиоцин |
|
Субъединица В |
Микроцин J17 |
||
|
Синтез клеточной стенки |
Синтез пептидогликана |
Пенициллинсвязывающие белки |
Бета-лактам |
|
MurA |
Фосфомицин |
||
|
ЛПС |
Полимиксин |
||
|
Аланинреацемаза и D-аланил-D-аланинлигаза |
D-циклосерин |
* По [26].
Формирование резистентных к антибиотикам биопленок — основная стратегия противодействия грамотрицательных бактерий стрептомицетам. Приобретение резистентности к какому-то антибиотику ведет к изменению реакции бактерии на определенный сигнал. Антибиотикорезистентные мутанты бактерий, также как и исходные чувствительные штаммы, реагируют на данный антибиотик. Но набор транскриптов у них иной, чем у исходных штаммов. Спонтанное приобретение резистентности к тем или иным антибиотикам способствует образованию других бактериальных экотипов [18].
Мобильные генетические элементы. Древность генетических механизмов биосинтеза антибиотиков предполагает наличие не менее древних генетических механизмов защиты от них. Распространение генов антибиотикорезистентности между бактериями происходит благодаря активности мобильных генетических элементов. Их два типа: генетические элементы, которые могут самостоятельно перемещаться между бактериями (конъюгативные плазмиды и конъюгативные транспозоны); и генетические элементы, перемещающиеся в пределах бактериальной клетки (по хромосоме, от хромосомы к плазмиде и наоборот: транспозоны, генные кассеты интегроны и др.). Плазмиды и конъюгативные транспозоны являются своеобразной платформой, на которой посредством различных рекомбинационных систем бактериальной клетки происходит сборка и сортировка генов антибиотикорезистентности. В табл. 2 дана характеристика мобильных генетических элементов бактерий, вовлеченных в распространение генов антибиотикорезистентности в природе.
Таблица 2. Характеристика мобильных генетических элементов бактерий, вовлеченных в распространение генов антибиотикорезистентности в природе*
|
Элемент |
Характеристики |
Роль в распространении генов резистентности |
|
Конъюгативные плазмиды |
Кольцевые, автономно реплицирующиеся генетические элементы, передающие гены между бактериями благодаря конъюгации |
Перенос генов резистентности; мобилизуют перенос других генетических элементов, включающих гены резистентности |
|
Конъюгативные транспозоны |
Интегрирующиеся элементы, которые могут «вырезаться» из хромосомы в виде нереплицирующегося кольцевого производного, способного к конъюга-ции |
Такая же |
|
Мобилизуемые плазмиды |
Носители генов, которые могут переноситься между бактериями благодаря конъюгациионному аппарату конъюгативных плазмид |
Перенос генов резистентности |
|
Нерепликативные единицы Bacteroides |
Интегрированные в геном бактероидов элементы, которые самостоятельно не способны из него «вырезаться» и переноситься между бактерииями; но эти процессы могут быть иници-ированы конъюгативными транс-позонами |
Такая же |
|
Транспозоны |
Могут перемещать фрагмент ДНК из одного участка генома бактерии в другой |
Перемещение генов антибиотикорезистентности от плазмиды к хромосоме и наоборот |
|
Генные кассеты |
Кольцевые нереплицирующиеся ДНК-сегменты, включающие только ORF; интегрируются в интегроны |
Включение генов резистентности |
|
Интегрон |
Интегрировавшийся в хромосому бактерии фрагмент ДНК, включающий ген интегразы, промотор и сайт интеграции для генных кассет |
Формирование кластеров генов резистентности, находящихся под контролем промотора интегрона |
|
Инсерционные криптические последовательности (ISCR-элементы) |
Образование комплексных интегронов первого класса |
Мобилизация генов, прилега-ющих к ISCR-элементу |
*По [19].
Мобильные генетические элементы участвовали в переносе генов резистентности к антибиотикам между бактериями еще до внедрения антибиотиков в клиническую практику. Описан штамм кишечной палочки, выделенный до 1937 г., содержащий плазмиду (R-фактор), определяющую устойчивость к тетрациклину и стрептомицину [21].
Транспозоны (Tn) — мобильные генетические элементы, несущие структурные гены, детерминирующие функции, не связанные с самим процессом перемещения между бактериями. Отдельные транспозоны включают гены антибиотикорезистентности, различающиеся между собой по структуре, происхождению и механизмам транспозиции. Механизмы перемещения транспозонов по геному бактерии не требуют гомологии между их ДНК и ДНК хромосомы бактерии в участках интеграции, хотя для некоторых транспозонов обнаружены предпочтения по интеграции среди таких участков. Известны транспозоны двух типов: 1) представляющие собой модульные системы. Их называют композитными транспозонами (composite transposons). Они включают пару IS-элементов и между ними — неспособную к транспозиции последовательность ДНК, содержащую структурный ген, изменяющий фенотип бактерии (рис. 1);
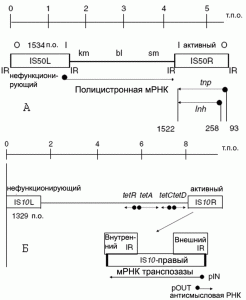
Рис. 1. Композитные транспозоны. А — Схема транспозона Tn5, включающего гены резистентности к канамицину (km), блеомицину (bl) и стрептомицину (sm). O и I — обозначения наружной и внутренней границ терминального инвертированного элемента IS50 (L — левый; R — правый), вмещающих короткие терминальные инвертированные повторы (IRs), определяющие границы IS50 и генов резистентности к антибиотикам. Б — Схема транспозона Tn10, включающего ген резистентности к тетрациклину. IS10 — инвертированный терминальный повтор. IS10L — левая половина IS10, представляющая собой копию IS10, нефункционирующую из-за множественных мутаций в гене транспозазы. IS10R — правосторонняя копия IS10, кодирующая активную транспозазу и антисмысловую молекулу РНК, снижающую экспрессию гена транспозазы. tetA — ген, кодирующий резистентность к тетрациклину по типу «выкачивающего насоса» («efflux pump»); tetC и D — гены, корегулируемые с tetA; tetR — ген, кодирующий транскрипционный репрессор, необходимый для индуцибельной экспрессии тетрациклинового «efflux pump» TetA. По [6]. Черными кружками показаны промоторы, п.о. — пары оснований, т.п.о. — тысяча пар оснований.
2) представляющие собой комплексные системы, в которых транспозиционная и нетранспозиционная функция не отражена четким модульным расположением нуклеотидных последовательностей. Транспозоны этой группы (complex transposons) более древние, чем композитные. Они имеют следы множественных рекомбинационных актов, включая вставки и делеции. Последние приходятся на участки, не имеющие отношения к транспозиции, что делает такие транспозоны компактными и увеличивает частоту их транспозиции (рис. 2).
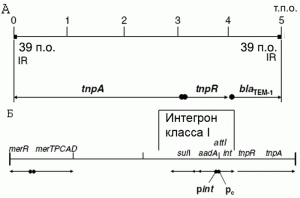 Рис. 2. Комплексные транспозоны. А — Схема транспозона Tn3, включающего гены резистентности к ампициллину и к некоторым другим антибиотикам бета-лактамного ряда. IR обнаружены по краям участка транспозона, необходимого для транспозиции; tnpA — ген, кодирующий компонент транспозазы; tnpR — ген, кодирующий сайт-специфическую рекомбиназу, позволяющую перемещение коинтегрированной структуры, образовавшейся в результате транспозиции; blaTEM-1 — ген, кодирующий TEM-1 бета-лактамазу. Б — Схема транспозона Tn21, включающего гены резистентности к стрептомицину, спектиномицину, сульфониламидам и ионам ртути: merTPCAD — гены, кодирующие резистентность к ионам ртути и отдельным органо-ртутным соединениям; merR — ген, кодирующий транскрипционный репрессор индуцибельного mer-оперона; sul1 — ген, кодирующий резистентность к сульфо-ниламидам; aadA1 — ген, кодирующий резистентность к стрептомицину и спекти-номицину; int — ген интегразы; attI — вставочный сайт для генной кассеты интегрона; tnpA — ген, кодирующий транспозазу Tn21; tnpR — ген, кодирующий сайт-специфическую рекомбиназу; рint — int-promoter (промотор для интегразы); Pc — промотор для кассеты интегрона и sul1. Стрелки на обеих схемах показывают направление и протяженность транскрипции. Черными кружками показаны промоторы, п.о. — пары оснований, т.п.о. тысяча пар оснований. По [6].
Рис. 2. Комплексные транспозоны. А — Схема транспозона Tn3, включающего гены резистентности к ампициллину и к некоторым другим антибиотикам бета-лактамного ряда. IR обнаружены по краям участка транспозона, необходимого для транспозиции; tnpA — ген, кодирующий компонент транспозазы; tnpR — ген, кодирующий сайт-специфическую рекомбиназу, позволяющую перемещение коинтегрированной структуры, образовавшейся в результате транспозиции; blaTEM-1 — ген, кодирующий TEM-1 бета-лактамазу. Б — Схема транспозона Tn21, включающего гены резистентности к стрептомицину, спектиномицину, сульфониламидам и ионам ртути: merTPCAD — гены, кодирующие резистентность к ионам ртути и отдельным органо-ртутным соединениям; merR — ген, кодирующий транскрипционный репрессор индуцибельного mer-оперона; sul1 — ген, кодирующий резистентность к сульфо-ниламидам; aadA1 — ген, кодирующий резистентность к стрептомицину и спекти-номицину; int — ген интегразы; attI — вставочный сайт для генной кассеты интегрона; tnpA — ген, кодирующий транспозазу Tn21; tnpR — ген, кодирующий сайт-специфическую рекомбиназу; рint — int-promoter (промотор для интегразы); Pc — промотор для кассеты интегрона и sul1. Стрелки на обеих схемах показывают направление и протяженность транскрипции. Черными кружками показаны промоторы, п.о. — пары оснований, т.п.о. тысяча пар оснований. По [6].
Транспозоны реагируют на изменения во внешней среде, окружающей бактерию. Например, частота транспозиции транспозона Тn501 существенно увеличивается при наличии в среде ртути, а транспозона Тn551 — в присутствии эритромицина. Примеры транспозонов, способных перемещать между бактериями гены антибиоти-корезистентности, приведены в табл. 3.
Таблица 3. Транспозоны, способные перемещать между бактериями гены антибиотикорезистентности*
|
Транспозон |
Размер (т.п.о.) |
Терминальные элементы |
Маркеры** |
|
Композитные транспозоны |
|||
|
Грамотрицательные бактерии |
|||
|
Tn5 |
5,7 |
IS50 (IR) |
KmBISm |
|
Tn9 |
2,5 |
IS1 (DR) |
Cm |
|
Tn10 |
9,3 |
IS10 (IR) |
Tc |
|
Tn903 |
3,1 |
IS903 (IR) |
Km |
|
Tn1525 |
4,4 |
IS15 (DR) |
Km |
|
Tn2350 |
10,4 |
IS1 (DR) |
Km |
|
Грамположительные бактерии |
|||
|
Tn4001 |
4,7 |
IS256 (IR) |
GmTbKm |
|
Tn4003 |
3,6 |
IS257 (DR) |
Tm |
|
Комплексные транспозоны |
|||
|
Грамотрицательные бактерии |
|||
|
Tn1 |
5 |
38/38 |
Ap |
|
Tn3 |
5 |
38/38 |
Ap |
|
Tn21 |
20 |
35/38 |
SmSuHg |
|
Tn501 |
8,2 |
35/38 |
Hg |
|
Tn1721 |
11,4 |
35/38 |
Tc |
|
Tn3926 |
7,8 |
36/38 |
Hg |
|
Грамположительные бактерии |
|||
|
Tn551 |
5,3 |
35 |
Ery |
|
Tn917 |
5,3 |
38 |
Ery |
|
Tn4451 |
6,2 |
12 |
Cm |
* По [6].
**Ap — ампициллин, BI — блеомицин, Cm —хлорамфеникол, Ery — эритромицин, Gm — гентамицин, Hg — ртуть, Km — канамицин, Sm — стрептомицин, Su — сульфаниламиды, Tc — тетрациклин, Tb — тобрамицин, Tm — триметоприм.
Интегроны и генные кассеты. Бактериальные интегроны представляют собой генные системы, которые вместо транспозиции (как это делают транспозоны) используют для распространения по геному бактерии сайт-специфическую рекомбинацию. Интегроны включают специальную рекомбинационную систему, кодирующую фермент интегразу (ген int), осуществляющий сайт-специфическую рекомбинацию; и сайт, в котором находится короткая последовательность ДНК — генная кассета [17]. Такое название она получила потому, что в наибольшей степени приспособлена только для отдельного гена, вставленного посредством интегразы. В процессе перемещения от одного интегрона к другому или от одного сайта в интегроне к другому сайту в том же интегроне, генная кассета существует как небольшая автономная и неспособная к репликации двунитевая кольцевая молекула ДНК [7]. Интегроны очень древние генетические элементы. Кроме генов антибиотикоустойчивости кассеты, захватываемые интегронами и суперинтегронами, могут содержать гены, кодирующие факторы патогенности, гены метаболизма, или гены, кодирующие рестрикционные ферменты. Различные генные кассеты содержат интеграционные сайты (attC), которые негомологичны друг другу. Интегроны бактерий различных видов, даже принадлежащих одному роду, могут содержать разные генные кассеты [2].
Большинство интегронов антибиотикорезистентности соответствуют мобильной генетической структуре, известной как интегроны класса 1 (class 1 integron). Они включают два концевых невариабельных региона, называемых константными последовательностями (constant sequences, CS), и высоковариабельный центральный участок. В одном конце интегрона — 5'-CS, обычно находятся: int — ген интегразы; attI — рекомбинационный сайт (локус) для кассеты; и промотор, от которого экспрессируются гены кассеты. В другом конце — 3'-CS, находится часть гена qacE∆1, который, будучи интактным несет устойчивость к четвертичным аммониевым соединениям. За ним расположен ген sul, определяющий резистентность микроорганизма к сульфаниламидам, и два других гена с неустановленной функцией, обозначенных как orf5 и orf6 (т.е. открытые рамки считывания 5 и 6). CS-регионы фланкируют вариабельные регионы и последовательность, включающую генные кассеты отдельного интегрона. Количество генных кассет у разных интегронов различное. Интегроны первого класса можно представить в виде следующей формулы:
intI attI (r59b)n qacE ∆1 sul1 orf5 orf6,
где r59b соответствует кассете резистентности, n показывает количество генных кассет, интегрировавшихся в локус attI [7].
Кассеты генов резистентности не содержат промоторы, от которых может начаться их экспрессия. Промотор для кассеты является частью интегрона. Поэтому вставки кассет в интегрон должны быть обязательно ориентированы таким образом, что бы старт гена, расположенного на кассете, начинался вблизи от int. Генные кассеты могут быть вставлены в сайт attI одна после другой, придавая бактерии резистентность к различным антибиотикам. Приобретение интегроном кассеты, дополнительной к уже имеющимся, создает новый интегрон (рис. 3).
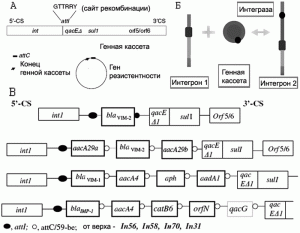 Рис. 3. Интегроны и генные кассеты. A — Схема интегрона резистентности класса 1. Б — Схема поглощения генной кассеты бактериальным интегроном. В — Примеры организации генной кассеты в бактериальных интегронах класса 1. int1 — ген итегразы класса 1; qac — ген, кодирующий устойчивость к четвертичным аммониевым соединениям; attI — вставочный сайт для генной кассеты; attC — вставочная последовательность генной кассеты; qacE∆1 — усеченная версия гена qacE; sul1 — ген, несущий резистентность к сульфаниламидам; orf — возможно ген с неустановленной функцией; blaVIM — ген, кодирующий VIM металло-бета-лактамазу; aacA, aadA, aph — гены, кодирующие резистентность к аминогликозидам; cat — ген, кодирующий резистентность к хлорамфениколу. По [6].
Рис. 3. Интегроны и генные кассеты. A — Схема интегрона резистентности класса 1. Б — Схема поглощения генной кассеты бактериальным интегроном. В — Примеры организации генной кассеты в бактериальных интегронах класса 1. int1 — ген итегразы класса 1; qac — ген, кодирующий устойчивость к четвертичным аммониевым соединениям; attI — вставочный сайт для генной кассеты; attC — вставочная последовательность генной кассеты; qacE∆1 — усеченная версия гена qacE; sul1 — ген, несущий резистентность к сульфаниламидам; orf — возможно ген с неустановленной функцией; blaVIM — ген, кодирующий VIM металло-бета-лактамазу; aacA, aadA, aph — гены, кодирующие резистентность к аминогликозидам; cat — ген, кодирующий резистентность к хлорамфениколу. По [6].
Разнообразие генных кассет трудно оценить. Недавно были идентифицированы генные кассеты, включающие гены, кодирующие металло-бета-лактамазы, придающие бактерии устойчивость к таким мощным карбапенем-бета-лактамам, как имипинем и меропинем (см. рис. 3В). Известны суперинтегроны, включающие десяток генных кассет, однако к деятельности человека они отношения не имеют. Среди бактерий, имеющих клиническое значение, большинство интегронов содержит менее пяти генных кассет [16].
Инсерционные криптические последовательности (ISCR-elements, IS-cryptic sequences). Это небольшие криптические последовательности, по размеру сходные со многими IS-элементами. Но у них совершенно иной, чем у транспозонов механизм транспозиции, названный транспозицией катящегося кольца (rolling circle transposition). Он объединяет RC-репликацию[1], используемую отдельными бактериальными плазмидами и бактериофагами, и рекомбинацию транспозиции IS-элементов[2] [11, 23].
ISCR-элементы впервые обнаружены как последовательности, ассоциирующиеся с интегронами класса 1, но при этом от них отличающиеся. Большинство из IS-элементов имеют четкие границы благодаря коротким инвертированным нуклеотидным повторам (см. рис. 1), функционально равнозначащим и заменяемым. Они действуют как сайты связывания и рассечения для родственной транспозазы. Большинство, если не все из комплексных транспозонов, имеют те же характеристики. В противоположность им, ISCR-элементы утратили концевые терминальные повторы, характерные для IS-элементов. Их терминальные последовательности обозначены как oriIS и terIS. Они служат уникальными сайтами для инициации и терминации репликационной стадии транспозиции соответственно. Важной особенностью этих систем, имеющих отношение к распространению генов антибиотикорезистентности среди бактерий, является то, что их репликация не является точной. В процесс репликации ISCR-элемента может вовлекаться ДНК бактерии, прилегающая к terIS за пределами инсерционной криптической последовательности. Поэтому вместе с ISCR-элементом может быть транспозирована последовательность в несколько раз большая, чем он сам, но всегда прилегающая к terIS [23]. То есть мобилизация ДНК является характерным признаком механизма RC-транспозиции ISCR-элемента; и мобилизована может быть любая ДНК, прилегающая к terIS. Этот механизм можно считать ключевым для образования комплексных интегронов первого класса (рис. 4).
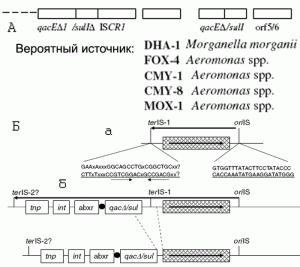 Рис. 4. Комплексные бактериальные интегроны. А — Примеры комплексных бактериальных интегронов первого класса с копиями ISCR1 и дупликациями 3'-CS. Пунктирная линия показывает 5'-CS и вариабельные регионы интегронов 1 класса, ставшие частью комплексных интегронов. DHA-1, FOX-1, CMY-1,8, MOX-1 — гены, кодирующие бета-лактамазы, которые придают бактерии резистентность к третьему поколению цефалоспоринов, вероятно рекрутированных из хромосом перечисленных бактерий. Другие обозначения см. в подрисуночном тексте к рис. 3. Б — Мобилизация интегронов первого класса посредством ISCR1. (a) границы ISCR1 очерчены через терминальные последовательности terIS-1 и oriIS. Наличие этих терминальных последовательностей у интегрона предполагает, что копии ISCR1 были транспозированы в сайт, близкий к 3'-CS-концу интегрона первого класса; (б) затем делецией (показана пунктирными линиями) удалена часть 3'-CS (включая orf5,6), образуя характерную 3'-CS-ISCR1-перестановку в интегроне первого класса. Теперь границы ISCR1 очерчены терминальными последовательностями terIS-2 и oriIS. По [6].
Рис. 4. Комплексные бактериальные интегроны. А — Примеры комплексных бактериальных интегронов первого класса с копиями ISCR1 и дупликациями 3'-CS. Пунктирная линия показывает 5'-CS и вариабельные регионы интегронов 1 класса, ставшие частью комплексных интегронов. DHA-1, FOX-1, CMY-1,8, MOX-1 — гены, кодирующие бета-лактамазы, которые придают бактерии резистентность к третьему поколению цефалоспоринов, вероятно рекрутированных из хромосом перечисленных бактерий. Другие обозначения см. в подрисуночном тексте к рис. 3. Б — Мобилизация интегронов первого класса посредством ISCR1. (a) границы ISCR1 очерчены через терминальные последовательности terIS-1 и oriIS. Наличие этих терминальных последовательностей у интегрона предполагает, что копии ISCR1 были транспозированы в сайт, близкий к 3'-CS-концу интегрона первого класса; (б) затем делецией (показана пунктирными линиями) удалена часть 3'-CS (включая orf5,6), образуя характерную 3'-CS-ISCR1-перестановку в интегроне первого класса. Теперь границы ISCR1 очерчены терминальными последовательностями terIS-2 и oriIS. По [6].
Такой интегрон имеет две особенности: 1) приблизительно половину его структуры занимает последовательность ДНК интегрона 1 класса, начавшаяся от 5'-CS-конца; 2) концевая последовательность 3'-CS и повтор вариабельного региона «следуют» через копию ISCR1. За ней находится другой вариабельный регион, давший прибежище различным генам резистентности, включая blaCMY- и blaCTX-варианты, qnrA- и dfrA-варианты, и catAII, которые несут резистентность к длинному ряду цефалоспоринов, флюорохинолонов (таких как ципрофлоксацин), триметаприму и хлорамфениколу. Эти вариабельные регионы находятся в «повернутом состоянии» за повтором [24].
Механизмы резистентности к антибиотикам у бактерий. Их можно классифицировать следующим образом: 1) модификация антибиотиков (другое название процесса — детоксикация). Заключается в разрушении антибиотика еще до его проникновения в цитоплазму клетку (внешняя среда, периплазматическое пространство грамотрицательных бактерий). При этом мишени антибиотиков в цитоплазме клетки остаются интактными. Осуществляется бактерией с помощью специфических ферментов, расщепляющих антибиотик до структур, не представляющих для нее опасности; 2) уменьшение проницаемости стенки бактерии для антибиотиков и/или выкачивание его из клетки («efflux pump») быстрее, чем антибиотик поразит свои мишени. Аналогичным образом действует судовая помпа, выкачивающая из трюма корабля забортную воду; 3) структурные изменения в молекулах, являющихся мишенями для антибиотиков. Проникший в клетку антибиотик не находит свои мишени и не может блокировать биохимические процессы; 4) продукция бактерией альтернативных мишеней, которые резистентны к ингибирующему действию антибиотика. Они связывают антибиотик и лишают его возможности поразить настоящие мишени. Обычно в качестве ложных целей выступают ферменты (рис. 5).
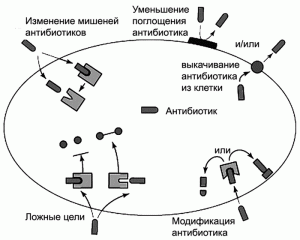
Рис. 5. Основные механизмы резистентности к антибактериальным препаратам у бактерий. По [14].
Устойчивость к антибиотикам, обусловленная плазмидами, преимущественно обеспечивается ферментами, модифицирующими антибиотики. Устойчивость к сульфаниламидам и триметоприму[3] вызвана тем, что плазмиды детерминируют дублирующие ферменты биосинтеза витаминов, нечувствительные к этим лекарственным препаратам. Но и для других механизмов резистентности показана возможность ее передачи посредством мобильных генетических элементов. Даже структурные изменения мишеней для антибиотиков могут быть вызваны вставочной активностью транспозонов. В обобщенном виде механизмы действия антибактериальных препаратов и механизмы резистентности к ним у бактерий приведены в табл. 4.
Таблица 4. Механизмы действия антибактериальных препаратов и резистентности к ним у бактерий*
|
Группа антибактериальных препаратов |
Препараты группы |
Механизм действия |
Механизмы резистентности |
|
Аминогликозиды |
Стрептомицин, гентамицин, тобрамицин, амикацин |
Ингибируют синтез белка путем связывания с частью субъединицы 30S бактериальной рибосомы
Большинство из них обладают бактерицидным действием (например, вызывают гибель бактериальных клеток) |
Модифицирующие ферменты (ацетилирование, аденилирование, фосфорилирование). Пониженная проницаемость или зависимое от энергии поглощение. Пониженное связывание антибиотика рибосомами |
|
Бацитрацин |
|
Ингибирует продуцирование клеточной оболочки путем блокирования этапа в процессе (рециклинг носителя мембранного липида), необходимого для добавления новых субъединиц клеточной оболочки. |
Пониженная проницаемость |
|
Бета-лактамные антибиотики |
Пенициллины: ампициллин, амоксициллин, тикарциллин. Цефалоспорины: цефтриаксон, цефокситин, цефалексин, цефтазидим. Монобактамы: азтреонам Карбепенемы: имипенем, меропенем |
Ингибируют образование бактериальной клеточной оболочки путем блокирования перекрестного связывания структуры клеточной оболочки в пенициллин-связывающих белках (пептидогликановые синтетические ферменты) |
Измененная мишень (пенициллин-связывающий белок). Пониженная проницаемость бета-лактамаз, модификация бета-лактамаз |
|
Хлорамфеникол |
|
Блокирует перенос аминокислот в пептидные цепи в субъединице 50S бактериальной рибосомы; ингибирует синтез белка |
Пониженная проницаемость. Активный отток. Инактивирующий фермент (ацетилирование) |
|
Гликопептиды |
Ванкомицин |
Препятствует развитию клеточной оболочки путем блокирования прикрепления новых субъединиц клеточной оболочки (мурамил-пентапептиды) |
Измененный сайт связывания предшественника пептидогликана
|
|
Линкосамиды |
Клиндамицин, линкомицин |
Блокируют перенос аминокислот в пептидную цепь в субъединице 50S бактериальной рибосомы; ингибирует синтез белка |
Пониженное связывание рибосом (метилирование рибосомальной РНК). Пониженная проницаемость. Модифицирующие ферменты |
|
Макролиды |
Эритромицин, кларитромицин, азитромицин |
Ингибируют транслокацию субъединицы 50S бактериальной рибосомы на иРНК; ингибируют белок |
Пониженная проницаемость. Модифицирующие ферменты. Слабое связывание с рибосомами (метилирование рибосомальной РНК) |
|
Метронидазол |
|
Разрушает структуру нуклеиновой кислоты |
Изменение механизмов активации препарата |
|
Оксазолидононы |
Линезолид, эперезолид |
Ингибируют синтез белка в 23S рРНК субъединицы 50S бактериальной рибосомы |
Измененная мишень |
|
Хинолоны |
Ципрофлоксацин, левофлоксацин, офлоксацин, норфлоксацин, налидиксовая кислота, спарфлоксацин |
Блокируют синтез ДНК ДНК-гиразой, топоизомеразой внутривенно |
Изменение мишени (ДНК-гираза, топоизомераза внутривенно). Пониженная проницаемость. Активный отток |
|
Рифампицин |
|
Ингибирует синтез РНК ДНК-зависимой РНК-полимеразой и таким образом синтез белка |
Слабое связывание с РНК-полимеразой |
|
Сульфаниламиды
|
Сульфаметоксазол, сульфацетамид, сульфадоксин |
Конкурентное ингибирование синтеза дигидрофолата из р-аминобензойной кислоты в дигидроптероат-синтетазе |
Измененная дигидроптероат-синтетаза. Повышенный уровень р-аминобензойной кислоты. Пониженная проницаемость |
|
Стрептограмины |
Хинупристин/ далфопристин |
Блокируют вытеснение вновь синтезированных пептидных цепей из субъединицы 50S бактериальной рибосомы |
Слабое связывание с рибосомой (метилирование рибосомальной РНК). Пониженная проницаемость. Модифицирующие ферменты |
|
Тетрациклины |
Тетрациклин, окситетрациклин, доксициклин, миноциклин |
Ингибируют связывание переносимой РНК на субъединице 30S бактериальной рибосомы; ингибируют синтез белка |
Детоксикация препарата. Барьеры проницаемости. Активный отток. Измененная мишень (рибосома) |
|
Триметоприм |
|
Ингибирует восстановление дигидрофолата до тетрагидрофолиевой кислоты в дигидрофолат-редуктазе |
Измененная дигидрофолат-редуктаза. Повышенный уровень р-аминобензойной кислоты. Пониженная проницаемость |
* По [25].
Резистентность к пенициллинам и цефалоспоринам. В ее основе лежит разрушение пенициллинов обширной группой ферментов, называемых пенициллиназами или бета–лактамазами. Эти ферменты разрывают бета–лактамные связи в молекулах пенициллинов, приводя к образованию неактивных производных (рис. 6).
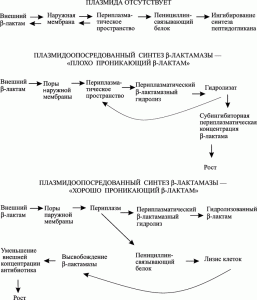 Рис. 6. Инактивация пенициллинов и цефалоспоринов бета-лактамазой. В обоих случаях бета-лактамная связь разрушается с помощью гидролитического механизма, но если образующаяся при этом пенициллоиновая кислота относительно стабильна, то соответствующий продукт гидролиза цефалоспоринов чрезвычайно нестабилен и распадается с образованием сложной смеси соединений. По [4].
Рис. 6. Инактивация пенициллинов и цефалоспоринов бета-лактамазой. В обоих случаях бета-лактамная связь разрушается с помощью гидролитического механизма, но если образующаяся при этом пенициллоиновая кислота относительно стабильна, то соответствующий продукт гидролиза цефалоспоринов чрезвычайно нестабилен и распадается с образованием сложной смеси соединений. По [4].
Наиболее распространенными среди бета-лактамаз являются бета-лактамазы TEM-1 и TEM-2, что связывают с локализацией их генов на транспозонах, переносимых между бактериями плазмидами. У грамположительных и грамотрицательных бактерий резистентность к пенициллинам (бета-лактамам) осуществляется преимущественно через детоксикацию антибиотика. У хорошо изученной грамположительной бактерии S. аureus основная часть синтезируемой бета-лактамазы уходит в окружающую среду и там разрушает бета-лактамные молекулы (рис. 7).
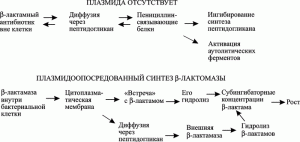 Рис. 7. Механизм развития плазмид-специфической резистентности к бета-лактамным антибиотикам у грамположительных бактерий. По [8].
Рис. 7. Механизм развития плазмид-специфической резистентности к бета-лактамным антибиотикам у грамположительных бактерий. По [8].
Фундаментальной причиной, способствующей закреплению в ходе эволюции за грамположительными бактериями устойчивости данного типа к антибиотикам, является отсутствие в их клеточной стенке периплазматического пространства. Уровень антибиотикорезистентности грамположительных микроорганизмов зависит от специфичности фермента и того его количества, которое он может позволить себе экспрессировать. Бета-лактамазы таких бактерий, как правило, имеют высокий аффинитет к бета-лактамным антибиотикам [8].
У грамотрицательных микроорганизмов деструкция бета-лактамных антибиотиков осуществляется в периплазматическом пространстве. Поэтому их уровень резистентности зависит от скорости, с которой бета-лактамазы проникают в периплазматическое пространство и скорости осуществляемого ферментами гидролиза. Такие бактерии обычно синтезируют меньшее количество фермента. Кроме того, он имеет меньшую субстратную специфичность (аффинитет), чем у грамположительных бактерий [8].
Большинство патогенных видов бактерий, встречающихся в стационарах, чувствительно, по меньшей мере, к одному классу бета-лактамовых антибиотиков [10].
Менее распространенной причиной резистентности бактерий к пенициллинам и цефалоспоринам могут быть мутации в генах пенициллинсвязывающих белков. Они приводят к пониженной аффинности этих белков к бета-лактамовым антибиотикам. Реже резистентность к таким антибиотикам вызывается их пониженным поглощением клеткой из-за изменений в ее оболочке или активного «откачивания» из бактериальной клетки проникшего антибиотика [10].
Резистентность к аминогликозидам. Плазмидная резистентность к аминогликозидным антибиотикам (гентамицин, стрептомицин и др.) связана либо с их энзимной модификацией, либо с нарушением проницаемости клеточной стенки бактерии для этих антибиотиков при отсутствии видимых признаков их энзимной модификации. Существует более 50 ферментов, способных к N-ацетилированию, О-фосфорилированию или О-нуклеотидилированию различных аминогликозидных антибиотиков [4,10].
Детоксикационный механизм плазмидной резистентности к антибиотикам данной группы характерен как для грамположительных, так и для грамотрицательных микроорганизмов [8]. Однако у последних резистентность носит более выраженный характер благодаря наличию полисахаридных внеклеточных слоев. Благодаря тому, что полисахариды несут отрицательный заряд (особенно это касается мукоидных штаммов псевдомонад), они способны связывать отдельные аминогликозы, препятствуя их дальнейшему проникновению в клетку. После проникновения через наружные слои клеточной стенки, аминогликозиды диффундируют через поры, расположенные в наружной мембране, и достигают пептидогликана, не представляющего для них серьезного барьера. Проникнув через клеточную стенку в периплазматическое пространство, аминогликозиды связываются с полярными группами фосфолипидов цитоплазматической мембраны. Здесь они вступают в контакт с модифицирующими энзимами. Модифицированный аминогликозид не способен связаться рибосомами и тем самым блокировать синтез белка в бактериальной клетке [8,14].
Резистентность к хлорамфениколу (левомицетину). Хлорамфеникол связывается с 50S рибосомной субъединицей и ингибирует этап пептидилтрансферазы при синтезе белка. Плазмидная резистентность к хлорамфениколу ассоциируется с наличием у них генов хлорамфениколацетилтрансферазы (cat). Широкое распространение устойчивости к этому антибиотику связано с распространением транспозона Tn9. Хлорамфениколацетилтрансферазы у грамотрицательных и грамположительных микроорганизмов обладают высокой степенью сходства по аминокислотным остаткам активного центра. Для резистентных к хлорамфениколу бактерий обеих типов характерна высокая детоксикационная активность в отношении этого антибиотика во внешней среде. Однако для некоторых грамотрицательных бактерий, например, псевдомонад, ее не наблюдается. У грамотрицательных бактерий иногда встречается пониженная проницаемость внешней мембраны к хлорамфениколу или его активный отток из клетки [8,14].
Резистентность к тетрациклину. Тетрациклины проникают в бактериальные клетки путем пассивной диффузии. Тетрациклин действует путем связывания с 30S рибосомальной субъединицей, приводя к ингибированию синтеза белка. Гены, определяющие устойчивость к тетрациклину (tet) грамотрицательных бактерий часто обнаруживаются в транспозоне Tn10, передаваемом между ними крупными конъюгативными плазмидами. У грамположительных микроорганизмов резистентность к тетрациклину обычно ассоциируется с плазмидами с молекулярной массой 2,7 и 2,8 МДа (например, у стафилококков). Плазмидная резистентность к тетрациклину связана с уменьшением его аккумуляции клеткой, обратным транспортом (у грамотрицательных — гены tetA–tetE, tetG и tetH; у грамположительных — гены tetK и tetL), внутриклеточной инактивацией (tetX) и защитой рибосом-мишеней (tetM или tetQ) [8,10].
Но большинство генов tet кодируют один из двух механизмов резистентности к тетрациклинам: либо отток антибиотика, либо рибосомную защиту. Рибосомная защита включает синтез белка, подобный фактору элонгации G. Он взаимодействует с рибосомой, не препятствуя синтезу белка, но и не давая тетрациклину ингибировать этот синтез. У некоторых видов бактерий обнаружено окислительное разрушение тетрациклина. Тем не менее детоксикационная инактивация антибиотика в природе не играет важную роль [10].
Резистентность к фторхинолонам. Фторхинолоновые антиактериальные препараты обнаруживают антибактериальное действие путем ингибирования некоторых бактериальных топоизомераз, а именно, ДНК-гиразы (бактериальная топоизомераза II) и топоизомеразы IV. Эти важные бактериальные ферменты изменяют топологию двунитевой ДНК (днДНК) в клетке. ДНК-гираза и топоизомераза IV являются гетеротетрамерными белками, состоящими из двух субъединиц, А и В. Гены, кодирующие субъединицы А и В, называются gyrA и gyrB (ДНК-гираза) или parC и parE (ДНК-топоизомераза IV) (grlA и grlB у S. aureus). ДНК-гираза является единственным ферментом, который может влиять на образование сверхспирали ДНК. Ингибирование этой активности фторхинолонами ассоциируется с быстрым убиванием бактериальной клетки. Топоизомераза IV также модифицирует топологию днДНК, но в то время как ДНК-гираза имеет, по-видимому, важное значение для поддержания образования сверхспирали, топоизомераза IV преимущественно ответственна за разделение нитей дочерней ДНК при делении клеток [10].
Механизмы бактериальной резистентности к фторхинолонам делятся на две основные категории: изменения в ферментах-мишенях для препарата и изменения, которые ограничивают проникновение препарата в мишень. У грамотрицательных микроорганизмов ДНК-гираза является, по-видимому, основной мишенью для всех хинолонов. У грамположительных микроорганизмов основной мишенью является топоизомераза IV или ДНК-гираза, в зависимости от рассматриваемого фторхинолона; т.е. структура хинолона определяет способ его антибактериального действия [10].
Плазмидную резистентность к хинолонам (plasmid-mediated quinolone resistance, PMQR) обнаружили Martinez-Martinez L. et al. [15]. Наиболее хорошо исследована резистентность бактерий к хинолонам, детерминируемая группой генов qnr. Они кодируют пентапептидповторяющиеся белки (pentapeptide repeat proteins), снижающие чувствительность бактерии к хинолонам посредством защиты от них комплекса днДНК и ДНК-гиразы или комплекса днДНК и топоизомеразы IV. Большинство qnr-генов (qnrA, qnrB и qnrS) идентифицированы на плазмидах размеров от 54 до более чем 180 т.п.о, обнаруживаемых в E. coli, Enterobacter spp., K. pneumoniae и Salmonella spp. Часто они ассоциированы с генами, кодирующими бета-лактамазы. Менее изученными PMQR-механизмами являются: 1) механизм, в работу которого вовлечена аминогликозидацетилтрансфераза с двумя аминокислотными заменами, позволяющими ей инактивировать ципрофлоксацин через ацетилирование; 2) кодируемый генами oqxAB и qepA «насос» («efflux pump»), обеспечивающий обратный транспорт проникшего в клетку хинолона [22].
Заключение
Проблема антибиотикорезистентности среди клинически значимых микроорганизмов уходит своими корнями в сложные экологические и эволюционные отношения между самими микроорганизмами, сложившиеся задолго до появления человека как биологического вида. Огромный потенциал генов антибиотико-резистентности накоплен в суперинтегронах, еще не вовлеченных в генетический обмен среди встречающихся в клинике микроорганизмов. Интерпретация же широкого распространения в клинике антибиотикорезистентных штаммов бактерий как явления, вызванного исключительно применением антибиотиков, сильно упрощает понимание данной проблемы и порождает иллюзию возможности ее решения путем ограничения использования антибиотиков в клинической практике. Целесообразно расширить круг исследуемых проблем, связанных с распространением антибиотикорезистентных патогенных микроорганизмов в клинике, включив в него процессы, благодаря которым происходит накопление и обмен генов антибиотикорезистентности среди бактерий в природных экосистемах.
Литература:
1. Брода П. Плазмиды. — М., 1982.
2. Смирнов Г.Б. Механизмы приобретения и потери генетической информации бактериальными геномами // Усп. совр. биол. — 2008. — Т. 128, № 1. — С. 52–76.
3. Титок М.А. Плазмиды грамположительных бактерий. — Минск, 2004.
4. Франклин Т., Сноу Дж. Биохимия антимикробного действия. — М., 1984.
5. Baltz R. H. Antimicrobials from Actinomycetes: back to the future // Am. Soc. Microbiol. — 2007. — V. 2. — P. 125–131.
6. Bennett P.M. Plasmid encoded antibiotic resistance: acquisition and transfer of antibiotic resistance genes in bacteria // Brit. J. Pharmacol. — 2008. — V. 153. — P. S347–S357.
7. Bennett P.M. Integrons and gene cassettes: a genetic construction kit for bacteria // J. Antimicrob. Chemother. — 1999. — V. 43. — P. 1–4.
8. Bryan L. Mechanisms of plasmid mediated drug resistance // Plasmids and Transposons. — N.Y., 1980. — P. 51–81.
9. Depardieu F., Podglajen I., Leclercq R. et al. Modes and modulations of antibiotic resistance gene expression // Clin. Microbiol. Rev. — 2007. — V. 20, № 1. — P. 79–114.
10. Fluit A.C., Visser M.R., Schmitz F. Molecular detection of antimicrobial resistance // Clin. Microbiol. Rev. — 2001. — V. 14, № 4. — P. 836–871.
11. Garcillian-Bracia M.P., de-la Crus F. Distribution of IS91 family insertion sequences in bacterial genomes: evolutionary implications // FEMS Microbiol. Ecol. — 2002. — V. 42, № 2. — P. 303–313.
12. Girgis H., Hottes A., Tavazoie S. Genetic architecture of intrinsic antibiotic susceptibility // PLoS ONE. — 2009. — V. 4, Is. 5. — e5629.
13. Goh E.B., Yim G., Tsui W. et al. Transcriptional modulation of bacterial gene expression by subinhibitory concentrations of antibiotics // Proc. Natl. Acad. Sci. USA. — 2002. — V. 99. — . 17025–17030.
14. Hawkey P.W. The origins and molecular basis of antibiotic resistance // BMJ. — 1998. — V. 317. — P. 557–560.
15. Martinez-Martinez L., Pascual A., Jacoby G.A. Quinolone resistance from a transferable plasmid // Lancet. — 1998. — V. 51. — P. 797–799.
16. Nordmann P., Poirel L. Emerging carbapenemases in gramnegative aerobes // Clin. Microb. Infect. — 2002 — V. 8. — P. 321–331.
17. Recchia G.D., Hall R.M. Gene cassettes: a new class of mobile element // Microbiology. — 1995. — V. 141. — P. 3015–3027.
18. Ryan R.P., Dow J.M. Diffusible signals and interspecies communication in bacteria // Microbiology. — 2008. — V. 154. — P. 1845–1858.
19. Salyers A., Abile-Cuevas C.F. Why are antibiotic resistance genes so resistant to elimination? // Antimicrob. Agents Chemother. — 1997. — V. 41, № 11. — P. 2321–2325.
20. Skold O. Resistance to trimethoprim and sulfonamides // Vet. Res. — 2001. — V. 32. — P. 261–273.
21. Smith D.H. R factor infection of Escherichia coli lyophilized in 1946 // J. Bact. — 1967. — V. 94. — P. 2071–2072.
22. Strahilevitz J., Jacoby G.A., Hooper D.C. et al. Plasmid-mediated quinolone resistance: a multifaceted threat // Clin. Microbiol. Rev. — 2009. — V. 22, № 4. — P. 664–689.
23. Tavakoli N., Comanducci A., Dodd H.M. et al. IS1294, a DNA element that transposes by RC transposition // Plasmid. — 2000. — V. 44, № 1. — P. 66–84.
24. Toleman M.A., Bennett P.M., Walsh T. Common regions e.g. orf513 and antibiotic resistance: IS91-like elements evolving complex class 1 integrons // J. Antimicrob. Chemother. — 2006. — V. 58. — P. 1–6.
25. Woods J.B. Antimicrobials for biological warfare agents // Biological weapons defense. N.J., — 2005. — P. 285–315.
26. Yim G., Wang H.H. Davies J. Antibiotics as signaling molecules // Phil. Trans. R. Soc. B. — 2007. — V. 362. — P. 1195–1200.
Библиографическое описание:
Супотницкий М.В. Механизмы развития резистентности к антибиотикам у бактерий // Биопрепараты. — 2011. — № 2. — С. 4–44.
Bibliographical description:
Supotnitskiy М.V. Mechanisms of Antibiotics Resistance in Bacteria // Biopreparats (Biopharmaceuticals) — 2011. — No. 2. — P. 4–11.
[1] Репликация — это синтез комплементарных нитей ДНК по матричной молекуле ДНК. Когда говорят о репликации «по типу катящегося кольца» (rolling circle model, RCM), то имеется ввиду ее вариант, наблюдаемый у плазмид. Особенностью данного типа репликации является её однонаправленность и асимметричный характер, выражающийся в разобщении синтеза ведущей и запаздывающей нитей плазмидной ДНК по времени, в результате чего образуется два продукта:1) двунитевая молекула ДНК, состоящая из родительской [-] и вновь синтезированной [+] нити и, 2) однонитевая молекула ДНК, представляющая собой вытесненную [+] родительскую нить. Затем на матрице вытесненной [+] нити синтезируется двунитевая молекула ДНК. Фрагменты ДНК соединяются ДНК-лигазой и суперскручиваются за счёт активности ДНК-гиразы. Более подробно о модели RCM см. в работе [3].
[2] Транспозиция принципиально иной процесс, чем репликация. Он представляет собой дупликацию мобильного генетического элемента, который остается в прежнем сайте, а его копия перемещается в сайт встраивания. Транспозиция мобильных генетических элементов включает этап репликации ДНК, ограниченный фланкирующими их участками.
[3] Сульфаниламиды и триметоприм — вещества немикробного происхождения, поэтому их относят к химиопрепаратам. Подробно о механизмах бактериальной резистентности к сульфаниламидам, можно ознакомиться по работам [8, 9, 12, 14, 20].

Михаил Васильевич Супотницкий
Российский микробиолог, полковник медицинской службы запаса, изобретатель, автор книг и статей по истории эпидемий чумы и других особо опасных инфекций, истории разработки и применения химического и биологического оружия. Заместитель главного редактора научно-практического журнала «Вестник войск РХБ защиты» Министерства обороны РФ.
Метки: 2011