Неисследованные тупики вакцинации
Аннотация. Полиморфизация человеческих популяций по мутантным аллелям генов, отвечающим за работу иммунной системы человека, приводит к развитию поствакцинальных осложнений, о которых еще несколько десятилетий назад ничего не знали, или они встречались очень редко. Необратимо изменился и характер самих эпидемических и пандемических процессов. ВИЧ-инфицированность населения привела к тому, что сегодня мы имеем дело уже не с удобными для проведения массовых вакцинаций эпидемическими монопроцессами, а с многокомпонентными процессами, имеющими множество неизвестных составляющих. В связи с тем, что в России не проводится обязательное массовое тестирование населения на ВИЧ-инфекцию, и прививаемому пациенту не всегда известно о его ВИЧ-статусе, то существует риск развития посвакцинальных осложнений, связанных как с диссеминацией живого компонента вакцины, так и провоцирования развития СПИДа антигенной стимуляцией инактивированным компонентом вакцины. Затруднить формирование иммунной прослойки в детских коллективах может низкая эффективность вакцинации у детей, внутриутробно экспонированных к антиретровирусным препаратам.
При разработке вакцин и проведении массовых вакцинаций также необходимо учитывать возможность появления осложнений, связанных с феноменами антигенного импринтинга и феномена антителозависимого усиления инфекции. Осложнения, в основе которых лежат эти феномены, могут проявиться через десятки лет после предыдущей вакцинации или эпидемии. Кроме того сама вакцинация, проведенная без их учета, способна утяжелить эпидемический процесс или вызвать развитие эпидемии близкородственного вируса в тех районах, где одновременно циркулируют этот вирус, и тот, против которого вакцинация проводилась.
Серьезную проблему для развития технологий конструирования современных вакцин и разработки безопасных стратегий вакцинации создают устаревшие знания по иммунологии и эпидемиологии, которые получают выпускники медицинских ВУЗов; и наличие среди представителей медицинской элиты лиц, связанных с фармацевтическим бизнесом и заинтересованных в том, что бы знания основной массы врачей в этих областях медицинской науки были управляемы и не превышали уровня, необходимого для работы в прививочном кабинете.
Библиографическое описание:
Супотницкий М.В. Неисследованные тупики вакцинации // Крымский журнал экспериментальной и клинической медицины. — 2011. — Т. 1, № 3–4. — С. 118–127.
Bibliographical description:
Supotnitskiy М.V. Unexplored deadlocks vaccination // Crimean Journal of experimental and clinical medicine. — 2011. — Vol. 1, № 3–4. — P. 118–127.
В руководствах по вакцинации поствакцинальные осложнения объясняются нарушениями «холодовой» цепи» при транспортировке и хранении вакцин или небрежностью, допущенной медицинским персоналом уже при проведении вакцинации [4]. Однако в научной литературе накапливаются данные, показывающие, что причины поствакцинальных осложнений могут иметь более сложный характер. А сами осложнения представлять собой сигналы о развитии долговременных или даже необратимых процессов, не учитываемых при планировании кампаний массовых вакцинаций. Целью данной работы является выявление генетических, эпидемических и иммунологических процессов, способных в ближайшем будущем создать серьезные препятствия для проведения массовых вакцинаций.
Если вернуться во времени на 200 лет назад и проанализировать, на каком популяционном фоне начинались Эдвардом Дженнером (1749–1823) первые массовые вакцинации против натуральной оспы, то можно прийти к выводу, что этот фон сильно изменился. На протяжении столетий среди эпидемических болезней доминировала натуральная оспа. В отличие от чумы, вспыхивавшей опустошительными эпидемиями раз в несколько десятилетий, и, даже, столетий, натуральная оспа присутствовала среди людей постоянно. Годовые колебания смертности различались в разы, но не на порядки. С 1667 г. по 1800 г. число умерших от оспы в Лондоне на 1000 умерших от других причин составляло в среднем 65 человек в год. Но это была иная оспа по «охватываемому» ею контингенту, по сравнению с тем, что мы наблюдали в ХХ столетии — т. е. до введения в практику массовых вакцинаций. «До Дженнера» оспа была исключительно детской болезнью (kinderblattern), которой болели все дети до года. Европейские врачи еще в начале XVIII в. придерживались точки зрения древних авторов Рази и Авиценны, что оспа является соматической болезнью. Она развивается у ребенка в результате брожения менструальной крови матери, которой тот питался, находясь в ее утробе.
Почему так долго держалось такое понимание причин возникновения натуральной оспы? Видимо потому, что оспой болели тогда все дети до года. Шведская и британская статистика XVII–XVIII вв. свидетельствует о том, что летальность среди детей, заболевших натуральной оспой, была постоянной на протяжении нескольких столетий, и не превышала 6–10 %. Только в XVIII в., когда появилось большое количество людей, не перенесших оспу в детстве, стало понятно, что оспа представляет собой инфекционную болезнь [1].
Современные данные о механизмах иммунного ответа у человека на вирус натуральной оспы говорят о том, что в первую очередь от оспы погибают индивидуумы, иммунная система которых не способна эффективно отвечать на инвазию вируса выработкой нейтрализующих антител. У таких пациентов оспа развивается в геморрагической форме, вирус в высоких титрах обнаруживается в фарингеальном тракте, увеличивая риск передачи болезни «по цепочке» [12]. То есть натуральная оспа на протяжении столетий осуществляла селективное давление на человеческие генотипы, изымая из популяций индивидуумы, имеющие генетические дефекты иммунной системы. Свой «вклад» в селекцию генотипов вносили другие контагиозные болезни — чума, грипп и корь.
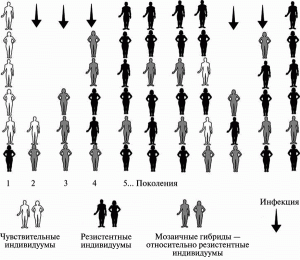 Рис. 1. Формирование возбудителями контагиозных инфекций популяционной резистентности к инфекционным болезням. За основу взята схема S.N. Rumyantsev [30]
Рис. 1. Формирование возбудителями контагиозных инфекций популяционной резистентности к инфекционным болезням. За основу взята схема S.N. Rumyantsev [30]
Поэтому к генетическим процессам, имеющим место в популяциях людей и способным привести к росту количества серьезных поствакцинальных осложнений, можно отнести полиморфизацию генов, ответственных за иммунные ответы на возбудители инфекционных болезней и антигены вакцин. Именно на сформированном возбудителями контагиозных инфекций популяционном генетическом фоне массовые вакцинации позволили достичь впечатляющих результатов в борьбе с инфекционными болезнями. Но у них имелась и обратная сторона — прекращение селективного давления на человеческие популяции со стороны возбудителей контагиозных инфекций привело к появлению в популяциях людей генотипов, существование которых еще два столетия назад было невозможным. В табл. 1 проводятся сведения об отдельных мутантных аллелях генов, участвующих в регуляции иммунного ответа у человека и о возможной их ассоциации с осложнениями после вакцинации.
Таблица 1
Мутантные аллели генов, участвующих в регуляции иммунного ответа у человека и возможная их ассоциация с осложнениями, возникающими после вакцинации*
|
Мутантная аллель |
Нарушение иммунного ответа |
Установленные осложнения при инфекционном процессе |
Возможные осложнения после вакцинации |
|
HLA DRB1*11 |
Пониженная секреция макрофагами интерферона-гама и IL-2 в ответ на антигенную стимуляцию |
Переход острой формы Ку-лихорадки в хроническую, развитие эндокардитов |
Развитие эндокардитов после вакцинации живыми вакцинами |
|
TNF2 |
Более сильный транскрипционный активатор, способствующий увеличению экспрессии TNFальфа |
Развитие церебральных форм малярии, развитие шока в ответ на инфекцию, вызванную хантавирусом, быстрое прогрессирование проказы, фатальные исходы менингококковых заболеваний, прогрессирование легочной формы туберкулеза |
Развитие шоковых состояний в ответ на введение инактивированных и химических вакцин, развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами |
|
NRAMP1 |
Врожденная недостаточность функции фагоцитоза |
Высокая чувствительность к туберкулезу, развитие открытых форм легочного туберкулеза, злокачественное течение туберкулеза |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
|
Мутация в гене рецептора IFN-γ R1 |
Врожденная недостаточность системы интерферона |
Диссеминация малопатогенных микобактерий, развитие фатального лептоменингита после вакцинации BCG, развитие BCG -остеомиелитов |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
|
VDR |
Врожденная низкая усвояемость витамина D |
Развитие легочной формы туберкулеза, остеопороз |
Развитие вакцино-ассоциированных инфекций после иммунизации живыми вакцинами, генерализация BCG |
В качестве примера разберем, каким образом мутации в генах, регулирующих работу иммунной системы человека, сказываются на результатах вакцинации вакциной BCG. В зависимости от типа наследования (рецессивного и доминантного), меняются клиника осложнения и шансы на возможность эффективной терапии. У представителей французского этноса мутация в рецепторе гамма-интерферона (IFN-γR1) приводит к диссеминации бацилл Кальмета-Герена и летальному лептоменингиту [24]; у японцев — к тяжелым формам остеомиелита, трудно поддающимся лечению [31]. Развитие атопического синдрома при вакцинации BCG ассоциируется с врожденной недостаточностью функции фагоцитов [5], диссеминация BCG ассоциируется с аутосомально-рецессивной недостаточность интерлейкина 12 (IL-12) [6] (рис. 2).
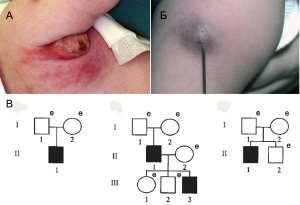 Рис. 2. Осложнения после вакцинации BCG. А Тяжелая гнойная лимфоаденопатия после вакцинации BCG. Б. Абсцесс после вакцинации BCG. По [8]. В. Полиморфизация гена IFN-γR1 на примере родословных трех японских семей. Поколения обозначены римскими цифрами, индивидуумы — арабскими цифрами. Пациенты с доминирующей частичной недостаточностью IFN-γR1, страдающие тяжелым BCG-остеомиелитом или подверженностью к микобактериальным инфекциям, показаны черными квадратами. e (examined) — проведено генетическое исследование на наличие мутации в гене IFN-γR1. Только у одного родственника обнаружено аутосомно-доминантное наследование мутации, у остальных они возникали спонтанно. По [31]
Рис. 2. Осложнения после вакцинации BCG. А Тяжелая гнойная лимфоаденопатия после вакцинации BCG. Б. Абсцесс после вакцинации BCG. По [8]. В. Полиморфизация гена IFN-γR1 на примере родословных трех японских семей. Поколения обозначены римскими цифрами, индивидуумы — арабскими цифрами. Пациенты с доминирующей частичной недостаточностью IFN-γR1, страдающие тяжелым BCG-остеомиелитом или подверженностью к микобактериальным инфекциям, показаны черными квадратами. e (examined) — проведено генетическое исследование на наличие мутации в гене IFN-γR1. Только у одного родственника обнаружено аутосомно-доминантное наследование мутации, у остальных они возникали спонтанно. По [31]
Родословные, приведенные на рис. 2В, показывают, что мутации в генах человека, участвующих в регуляции иммунного ответа, возникают спонтанно. Поэтому в отдельных человеческих популяциях происходит их постоянное накопление. Но какова частота в вакцинируемых популяциях детей с такими мутантными аллелями? Какую роль они сыграли в развитии уже установленных поствакцинальных осложнений? К сожалению, ответов на эти вопросы до сих пор нет. Вину же за все осложнения после вакцинаций массовое сознание возлагает на медицинские учреждения, где проводили вакцинацию.
Эпидемический процесс, с которым необходимо считаться при проведении массовых вакцинаций — ВИЧ/СПИД-пандемия. В России идет постоянный рост ВИЧ-инфицированности населения, в среднем на 5–10 % ежегодно. Первые массовые вакцинации, начатые в 1920-х гг., осуществлялись на совершенно ином эпидемическом фоне и были направлены на борьбу с отдельными моноэпидемиями и монопандемиями гриппа, кори, дифтерии и др. инфекций. Сегодня эти же инфекции развиваются на фоне распространения ВИЧ-инфекции и еще двух десятков ВИЧ-ассоциированных инфекций, т. е. на фоне многокомпонентного пандемического процесса, «мира без ВИЧ» уже не будет [3].
Официально в России на начало 2012 г. зарегистрировано более 600 тыс. ВИЧ-инфицированных граждан, однако их точное количество неизвестно. Не выявленный ВИЧ-статус у пациента создает угрозу для его жизни и для жизни окружающих. У ВИЧ-инфицированных возможны два варианта течения вакцинного процесса после вакцинации живыми вакцинами. Быстрая гибель вакцинированного пациента непосредственно от развившегося инфекционного процесса, например, в течение месяца после вакцинации в результате диссеминации вакцины BCG [34]; и «отложенная смерть» от обострения течения ВИЧ-инфекции, спровоцированного введением вакцины. Например, у 20-летнего пациента, вакцинированного живой противокоревой вакциной, через 10 мес развились легочные инфильтраты, в которых был обнаружен вакцинный штамм вируса кори (Moratan strain). Лечение специфическим иммуноглобулином и рибаверином оказалось неэффективным, болезнь прогрессировала и больной погиб [7]. Описаны и другие случаи гибели людей, вакцинированных живыми вакцинами на поздней стадии ВИЧ-инфекции [34].
В перспективе поменять все живые вакцины на инактивированные или субъединичные, не удастся: во-первых, такие вакцины у иммунокомпетентных людей дают только непродолжительный и неполный защитный эффект и прививки надо будет повторять; во-вторых, создание любой антигенной нагрузки у ВИЧ-инфицированного человека сопровождается риском активизации покоящихся CD4 Т-клеток, у которых с геномом интегрировался провирус ВИЧ. Жизненный цикл вируса в этом случае может возобновиться, и процесс перехода ВИЧ-инфекции в СПИД ускорится [3, 13].
То что иммунная система ВИЧ-инфицированных детей не может эффективно отвечать на введение вакцины, известно давно. Но у этой проблемы есть другая сторона. В случае беременности ВИЧ-инфицированным женщинам назначают антиретровирусную химиопрофилактику (АРВX), позволяющую в 4–20 раз увеличить частоту рождения ВИЧ-негативных детей. По сравнению с детьми, рожденными здоровыми матерями, и не экспонированными к антиретровирусным препаратам, дети, рожденные ВИЧ-инфицированными матерями, получавшими АРВX, на пике ревакцинаторного ответа слабее реагируют на дифтерийный анатоксин и коклюшный компонент АКДС-вакцины. У них синтезируется меньше антител изотипа IgG и всех его субклассов, а также IgA, но повышена продукция IgM. Их ответ отличается избыточной несбалансированной экспансией CD4+T- и γδ Т-клеток, что характерно для ранней стадии ВИЧ-инфекции. Они слабее формируют гиперчувствительность замедленного и немедленного типа к анатоксинам. Несостоятельность Т-клеток сохраняется до 10 лет. Количество детей, внутриутробно экспонированных к ВИЧ/АРВX, постепенно возрастает. В 2009 г. в России было примерно 170 тыс. ВИЧ-инфицированых молодых женщин. У них уже родилось 52 тыс. детей, из которых 32 тыс. благодаря АРВX не заразились ВИЧ [2]. Этот феномен практически не изучается. Детей, в случае отсутствия антител к ВИЧ, снимают с учета через полтора года наблюдения. О какой иммунной прослойке в детских коллективах можно будет говорить через несколько лет?
Другое следствие расширения ВИЧ-инфицированной прослойки среди населения — формирование эпидемических цепочек между ВИЧ-инфицированными детьми, случайно вакцинированными живыми вакцинами; и ВИЧ-инфицированными взрослыми. Имеются доказательства такой передачи M. bovis BCG [34].
В эпидемических процессах, казалось бы, давно изученных, например, гриппа или кори, в последние годы обнаружены отсутствующие в учебниках по эпидемиологии и иммунологии составляющие, действующие на уровне иммунной системы людей, но популяционно проявляющие себя как факторы, способные увеличить тяжесть эпидемического процесса и, даже, способствовать развитию других эпидемий. Это феномены антигенного импринтинга и антителозависимого усиления инфекции, сопровождающие массовые вакцинации и эпидемические процессы.
Феномен антигенного импринтинга (другое название — феномен первичного антигенного греха, phenomenon of original antigenic sin) состоит в том, что при повторном контакте иммунной системы с вирусом или вакциной, иммунная система может не воспринимать различия между вариантом эпитопа, с которым уже познакомилась ранее, и его новым вариантом. И тогда активизируются В-клетки памяти, «запомнившие» предыдущий антиген. Выработка антител происходит в отношении этого антигена, хотя реально иммунная система с ним не контактирует. Образующиеся антитела не способны нейтрализовать вирус, вызвавший инфекционный процесс, выработка же специфических антител к нему тормозится из-за подавления «наивных» В-клеток активизировавшимися В-клетками памяти. Этот феномен наблюдается при ВИЧ-инфекции, при гриппе, лихорадке Денге, лептоспирозе, малярии и энтеровирусной инфекции.
Феномен антигенного импринтинга имеет прямое отношение к проблеме обеспечения безопасности вакцинации. В 1953 г. F.M. Davenport et al. [10] при исследовании образцов сывороток крови, взятых от детей во время вспышки гриппа, обнаружили, что в сыворотке детей, переболевших гриппом до вакцинации, мало антител к вирусу, использованному для вакцинации, антитела образовались к вирусам гриппа, циркулировавшим ранее. В 1960-х гг. и позже этот феномен нашел многократное подтверждение в работах других исследователей [11, 14, 40].
В 1979 г. R.B. Couch et al. [9] обнаружили, что после вакцинации инактивированной гриппозной вакциной, полученной на основе штамма вируса A/Scotland/74 (H3N2), в сыворотке 82 % вакцинированных людей найдены антитела к вирусу A/HongKong/68 (H3N2), с которым они сталкивались ранее. Только в сыворотке 46 % вакцинированных присутствовали низкие уровни антител к вакцинному штамму A/Scotland/74.
W. Marine и J. Thomas [28] подтвердили феномен антигенного импринтинга в масштабном исследовании, выполненном на 687 добровольцах разных возрастов, перенесших грипп во время различных пандемий. Добровольцев вакцинировали живыми моновакцинами разных серотипов и изучали анамнестические ответы иммунной системы.
Антигенное расстояние между штаммами вирусов гриппа, необходимое для индукции антигенного импринтинга, неизвестно. Установлено только то, что этот феномен не наблюдается при последовательном заражении животных антигеннодалекими штаммами вируса гриппа [16, 25].
До последнего времени считалось, что вакцинация инактивированными гриппозными вакцинами позволяет избежать феномена антигенного импринтинга [41]. Однако в 2009 г. J.H. Kim et al. [25] в экспериментах на животных показали, что если проводить их последовательную вакцинацию инактивированными вакцинами, полученными на основе разных штаммов вируса гриппа H1N1 (PR8 и FM1), то при последующем заражении адаптированным штаммом вируса гриппа FM1, мыши оказываются менее защищенными от вируса, чем после иммунизации только одним инактивированным FM1. Титр вируса гриппа в легких мышей, вакцинированных сначала PR8, а затем FM1, был в 46 раз выше, чем у мышей, вакцинированных только инактивированным FM1. Интересно, что мыши, вакцинированные сначала инактивированной вакциной, а затем живой, демонстрируют выраженный феномен первичного антигенного греха. Последующее инфицирование животных вирулентным штаммом вируса вызывает у них слабый ответ нейтрализующих антител на этот вирус.
Феномен антигенного импринтинга обнаружен не только при инфекционных процессах, вызванных антигенно-дрейфующими вирусами, такими как ВИЧ или вирус гриппа, но и более стабильными вирусами, но циркулирующих, как множество разных серотипов и штаммов, например, при вспышках лихорадки Денге [17]. К тому же этот феномен имеет клеточную составляющую, основанную на Т-клетках памяти [26]. Последовательное введение мышам различных штаммов вируса лимфоцитарного хориоменингита (lymphocytic choriomeningitis virus, LCMV), вызывало у них образование CTL-клеток, специфичных только в отношении штамма LCMV, введенного первым [26].
К чему приводят массовые вакцинации против гриппа, осуществленные без учета феномена антигенного импринтинга, показали четыре эпидемиологических исследования распространения вируса так называемого «свиного» гриппа H1N1 в Британской Колумбии (провинция на западе Канады), выполненные в 2009 г. Оказалось, что риск развития гриппа у лиц, ранее вакцинированных тривалентной инактивированной гриппозной вакциной, созданной на основе штаммов вируса H1N1 (trivalent inactivated influenza vaccine, TIV), был даже большим, чем у лиц, ранее не вакцинированных [23, 32]. Но это отдельный случай, описанный добросовестными канадскими учеными, а что мы знаем о подобном развитии эпидемии у себя в стране?
Другой, упорно не замечаемый авторами учебников по иммунологии и эпидемиологии иммунологический феномен, встречающийся как при инфекционных процессах, так и как результат вакцинации и лечения иммуноглобулинами — антителозависимое усиление инфекции (antibody-dependent enhancement, ADE). Суть феномена состоит в том, что вирусспецифические антитела связывают вирус и посредством взаимодействия с рецепторами, расположенными на поверхности фагоцитирующих клеток усиливают его проникновение в эти клетки, а в отдельных случаях даже стимулируют его репликацию. Оба эти процесса приводят к утяжелению течения болезни. Почему это происходит? Любой антиген содержит несколько эпитопов, и на каждый из них иммунная система может вырабатывать антитела. Поэтому сыворотка пациента с развившимся инфекционным процессом, либо вакцинированного пациента, содержит не только «протективные антитела», как это можно прочитать в популярных учебниках по иммунологии и микробиологии, а смесь антител [33]:
нейтрализующих возбудитель инфекционной болезни в присутствии комплемента;
нейтрализующих возбудитель инфекционной болезни без комплемента;
усиливающих инфекционный процесс посредством увеличения адгезии возбудителя инфекционной болезни к фагоцитирующим клеткам через Fc-рецептор или рецептор комплемента[1];
усиливающих активацию вирусных белков путем изменения их конформации;
супрессирующих антивирусные ответы клетки на транскрипционном уровне;
оказывающих токсическое воздействие на клетку.
Репертуар этих антител варьирует в зависимости от биологических особенностей самого вируса, состояния иммунной системы человека и стадии инфекционного процесса.
Механизм антителозависимого усиления инфекции запускается тогда, когда конформация комплекса антитело-вирусный белок позволяет Fc-фрагментам антител взаимодействовать с Fc-рецептором или рецептором комплемента (C1q) на поверхности фагоцитирующей клетки. Антитела образуют мост между вирусом и этими рецепторами, облегчая оболочечному вирусу взаимодействие со специфическим рецептором на ее поверхности (рис. 3, В; рис. 4, А).
Безоболочечным вирусам (non-enveloped viruses), образовавшим комплекс с антителом, способным взаимодействовать с Fc-рецептором или рецептором комплемента (C1q), специфические рецепторы на поверхности клетки-мишени не требуются [33].
Подобным же образом С1 (компонент комплемента; его субъединица C1q имеет рецептор для связывания с Fc-фрагментом молекулы антитела) может связывать Fc-фрагмент антитела, инициируя классический путь активации комплемента, в результате чего активируется компонент комплемента С3, ковалентно (!) связывающийся или с антителом или с поверхностью вирусной частицы (рис. 4, В).
Образовавшийся комплекс способен взаимодействовать с рецепторами комплемента на поверхности клетки посредством С3, усиливая взаимодействие вируса с клеткой. Альтернативно C1q-субъединица непосредственно может перекрестно связывать вирусный белок и C1q-рецепторы (C1qR) на поверхности фагоцитирующих клеток (см. рис. 4, С). Все перечисленные эффекты находятся в зависимости от концентрации антител (см. рис. 3).
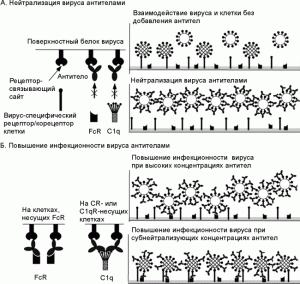 Рис. 3. Зависимость феномена нейтрализации вирусов и усиления инфекции от концентрации специфических антител. А. Нейтрализация вируса специфическими антителами. Если большинство функциональных сайтов вирусных белков блокировано антителами (левая панель), то при высоких концентрациях антител проникновение вируса в клетку ингибируется независимо от типа антител (нижняя правая панель).
Рис. 3. Зависимость феномена нейтрализации вирусов и усиления инфекции от концентрации специфических антител. А. Нейтрализация вируса специфическими антителами. Если большинство функциональных сайтов вирусных белков блокировано антителами (левая панель), то при высоких концентрациях антител проникновение вируса в клетку ингибируется независимо от типа антител (нижняя правая панель).
Б. Повышение инфекционности вируса специфическими антителами. Когда Fc-фрагмент нейтрализующего антитела оказывается способным связываться с FcR или C1q (левая панель), антитела могут усиливать инфективность вируса (virus infectivity) в субнейтрализующих концентрациях, при которых свободные вирусные белки могут инициировать проникновение вируса в клетку (нижняя правая панель). При высоких концентрациях нейтрализующих антител, связывание вируса с клетками происходит посредством Fc-фрагмента нейтрализующего антитела. C1q — субъединица белка комплемента С1. В составе молекулы C1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела. За основу взята схема A. Takada, Y. Kawaoka [33].
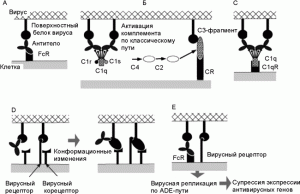 Рис. 4. Возможные механизмы развития феномена ADE для вирусных инфекций. А. Взаимодействие между антителом и FcR.
Рис. 4. Возможные механизмы развития феномена ADE для вирусных инфекций. А. Взаимодействие между антителом и FcR.
В. Фрагмент С3 комплемента (компонент комплемента, после присоединения которого весь этот комплекс приобретает способность прилипать к различным частицам и клеткам) и рецептор комплемента (complement receptor; CR) инициируют присоединение вируса к клетке.
С. Белки комплемента С1q и С1qR инициируют присоединение вируса к клетке (в составе молекулы C1q имеется рецептор для связывания с Fc-фрагментом молекулы антитела).
D. Антитела взаимодействуют с рецептор-связывающим сайтом вирусного белка и индуцируют его конформационные изменения, облегчающие слияние вируса с мембраной.
Е. Вирусы, получившие возможность реплицироваться в данной клетке посредством ADE, супрессируют антивирусные ответы со стороны антивирусных генов клетки. По [33]
Общие особенности вирусов, вызывающих феномен ADE, следующие: а) обычно такие вирусы реплицируются в макрофагах; б) они индуцируют продукцию большого количества антител с плохой способностью к нейтрализации гомологичных вирусов; в) способны к персистентной инфекции, характеризующейся продолжительной виремией [37].
В основном феномен ADE проявляется в ответ на образование антител изотипа IgG1 [19]. У людей имеются три типа рецепторов Fc, которые связывают человеческие IgG: это сиалогликопротеины FcγRI, FcγRII и FcγRIII (CD16). FcγRI наиболее представлен на моноцитах/макрофагах человека, и он связывает IgG с наибольшей авидностью. Поэтому ему принадлежит «лидерство» среди других рецепторов макрофагов в реализации феномена ADE. ADE, показанный в условиях in vitro, не обязательно воспроизводится в условиях in vivo [27].
Феномен ADE описан для ВИЧ и некоторых других ретровирусов, вызывающих болезни у животных, для возбудителей лихорадки Эбола, Марбург, гепатита С, кори, желтой лихорадки, энцефалита Западного Нила, лихорадки Денге и отдельных энтеровирусов.
C начала 1960-х гг., т.е. после начала массовых иммунизаций населения вакцинами против кори, инактивированными формалином, среди вакцинированных людей отмечаются случаи так называемой атипичной кори (т. е. кори, протекающей в тяжелой форме). В 2006 г. установлено, что в основе тяжелого течения кори у взрослых лежит феномен антителозависимого усиления инфекции, обусловленный наличием низких титров антител к гемагглютинину вируса (поверхностный белок Н) в крови пациента, оставшихся после вакцинации сделанной в детстве [21].
ADE при ВИЧ-инфекции показан W. E. Robinson et al. [29] и J. Homsy et al. [20]. Наиболее важным эпитопом оболочечного белка ВИЧ для развития C-ADE у ВИЧ-инфицированных людей является иммунодоминантный регион gp41. Развитие FcR-ADE происходит благодаря антителам к V3-петле gp120 [15]. У ВИЧ-инфицированных людей соблюдается определенная очередность проявления вариантов развития ADE. На ранней стадии инфекции феномен реализуется через V3-петлю gp120 (по типу FcR-ADE). По типу C-ADE феномен начинает проявляться перед клиническим прогрессированием ВИЧ-инфекции [35]. G. Fust [15] кратко суммировал клиническое значение феномена ADE для ВИЧ-инфекции — это прогрессирование инфекции; и облегчение переноса вируса от матери к плоду.
В 1990-х гг. с целью моделирования стратегий вакцинации против ВИЧ были проведены исследования по оценке эффективности вакцин против другой ретровирусной болезни — инфекционной анемии лошадей. Исследователи использовали виремию, как критерий тяжести болезни. У животных, вакцинированных инактивированной цельновирионной вакциной, высокоочищенным оболочечным гликопротеином вируса, а также рекомбинантной вакциной, полученной на основе поверхностного гликопротеина вируса инфекционной анемии лошадей, не удалось предотвратить развитие болезни. Во всех экспериментах авторы показали ее серьезное обострение у вакцинированных лошадей и пони, как следствие присутствия антител, индуцированных введением вакцины [22, 39]. У российских разработчиков ВИЧ-вакцин эти данные интереса не вызывают.
По мере углубления наших знаний механизмов иммунных ответов на инфекцию и вакцинацию, перечень подобных поствакцинальных осложнений будет расширяться. M. J. Wallace et al. [38], S. Thomas et al. [36] и J-F Han et al. [18] уже ставят вопрос о необходимости обязательного изучения феноменов антителозависимого усиления инфекции в процессе разработки, доклинического и клинического исследования вакцин, и при проведении массовых вакцинаций. Пока мы повторяем банальности столетней давности о «протективных антителах», и бесконечно уточняем общеизвестные факты, лидерство в конструировании вакцин следующего поколения, позволяющих избежать антителозависимого усиления инфекции, переходит к западным исследовательским коллективам.
Таким образом, есть серьезные основания считать, что массовые вакцинации в будущем ожидают большие трудности из-за роста поствакцинальных осложнений, не имеющих отношения к качеству самих вакцин. Из-за отсутствия селективного давления со стороны контагиозных инфекций происходит полиморфизация человеческих популяций по мутантным аллелям генов, отвечающих за работу иммунной системы человека. В популяциях накапливаются индивидуумы с мутантными аллелями генов, участвующими в регуляции иммунного ответа. Поэтому применяемая без проблем еще 30 лет назад вакцина, сегодня может вызвать труднообъяснимые осложнения.
ВИЧ-инфицированность населения изменила характер эпидемических и пандемических процессов. В настоящее время мы имеем дело уже не с монопроцессами, как еще 30 лет назад, а с многокомпонентными процессами, имеющими множество неизвестных составляющих. В связи с тем, что в России не проводится обязательное массовое тестирование населения на ВИЧ-инфекцию, и прививаемому пациенту не всегда известно о его ВИЧ-статусе, то существует риск развития посвакцинальных осложнений, связанных как с диссеминацией живого компонента вакцины, так и провоцирования развития СПИДа антигенной стимуляцией инактивированной вакцины. Кроме того, серьезно затруднить формирование иммунной прослойки в детских коллективах может низкая эффективность вакцинации у детей, внутриутробно экспонированных к антиретровирусным препаратам.
При разработке вакцин и проведении массовых вакцинаций также необходимо учитывать возможность появления осложнений, связанных с феноменами антигенного импринтинга и феномена антителозависимого усиления инфекции. Феномен антигенного импринтинга должен учитываться при разработке вакцин массового применения против вирусов, у которых оболочка содержит множество поверхностных эпитопов разной перекрестной специфичности, включая антигенно-дрейфующие вирусы, такие как вирус гриппа А и ВИЧ; и более стабильные вирусы, но циркулирующие конкурентно как множество разных серотипов и штаммов (вирус лихорадки Денге). Феномен антителозависимого усиления инфекции необходимо учитывать при разработке вакцин против вирусов, обычно реплицирующих в макрофагах, индуцирующих продукцию большого количества антител с плохой способностью к нейтрализации гомологичных вирусов и способных к персистентной инфекции, характеризующейся продолжительной виремией. Осложнения, связанные с этими феноменами, могут проявиться через десятки лет после предыдущей вакцинации или эпидемии. Кроме того сама вакцинация, проведенная без их учета, может утяжелить эпидемический процесс или вызвать развитие эпидемии близкородственного вируса в тех районах, где одновременно циркулируют этот вирус, и тот, против которого проводилась вакцинация.
Серьезную проблему для развития технологий конструирования современных вакцин и разработки безопасных стратегий вакцинации создают устаревшие знания по иммунологии и эпидемиологии, которые получают выпускники медицинских ВУЗов; и наличие среди представителей медицинской элиты лиц, связанных с фармацевтическим бизнесом и заинтересованных в том, что бы знания основной массы врачей в этих областях медицинской науки были управляемы и не превышали уровня, необходимого для работы в прививочном кабинете..
Список использованных источников
1. Губерт В. О. Оспа и оспопрививание. — СПб., 1896.
2. Кузьмина М.Н., Чепрасова Е.В., Свиридов В.В. с соавт. Попытка иммунокоррекции Аффинолейкином нарушений ревакцинаторного ответа на АКДС у ВИЧ-негативных детей, рождённых ВИЧ-инфицированными матерями после антиретровирусной химиопрофилактики // Биопрепараты. — 2010. — № 4. — С. 32–36.
3. Супотницкий М.В. Эволюционная патология. — М., 2009.
4. Ясинский А.А., Михеева И.В. Безопасность иммунизации // В кн. Вакцины и вакцинация. Национальное руководство. Под ред. В.В. Зверева, Б.Ф. Семенова, Р.М. Хаитова — М., — С. 137–161.
5. Alm J., Sanjeevi C.B., Miller E. N. et al. Atopy in children in relation to BCG vaccination and genetic polymorphisms at SLC11A1 (formerly NRAMP1) and D2S1471 // Genes and Immunity. — 2002. — Vol. 3. — P. 71–77.
6. Altare F., LammasD., Revy P. et al. Inherited Interleukin 12 deficiency in a child with bacille Calmette-Guerin and Salmonella enteritidis disseminated Infection // J. Clin. Invest. — 1998. — Vol. 102, № 12. — P. 2035-2040.
7. Angel J. B, Walpita P., Lerch R. A. et al. Vaccine-associated measles pneumonitis in an adult with AIDS // Ann. Intern. Med. — 1998. — Vol. 129. — P. 104–106.
8. Bolger T., O'Connell M., Menon A. et al. Complications associated with the bacille Calmette-Guerin vaccination in Ireland // Arch. Dis. Child. 2006. — Vol. 91. — P. 594–597 (doi: 10.1136/adc.2005.078972)
9. Couch R. B., Webster R. G. Cate T. R. et al. Efficacy of purified influenza subunit vaccines and relation to the major antigenic determinants on the hemagglutinin molecule // J. Infect. Dis. — 1979. — Vol. 140. — P. 553–559.
10. Davenport F. M., Hennessy A. V., Francis T. Epidemiologic and immunologic significance of age distribution of antibody to antigenic variants of influenza virus // J. Exp. Med. — 1953. — Vol. 98. — P. 641–656.
11. de Fazekas St., Webster R. G. Disquisitions on original antigenic sin, II: proof in lower creatures // J. Exp. Med. — 1966. — Vol. 124. — P. 347–361.
12. Downie A. W., McCarthy K. The antibody response in man following infection with viruses of the pox group. III. Antibody response in smallpox // J. Hyg. ( London ). — 1958. — Vol. 56. — P. 479–487.
13. Finzi D., Plaeger S. F., Dieffenbach C. W. Defective virus drives human immunodeficiency virus infection, persistence, and pathogenesis // Clinical and Vaccine Immunology. — 2006. — Vol. 13. — № 7. — P. 715 — 721.
14. Francis T. On the doctrine of original antigenic sin // Proc. Am. Philos. Soc. —1960. — Vol. 104. — P. 572–578.
15. Fust G . Enhancing antibodies in HIV infection // Parasitology. — 1997. — Vol. 115, Suppl: S 127—140.
16. Gulati U., Kumari K., Wu W. et al. Amount and avidity of serum antibodies against native glycoproteins and denatured virus after repeated influenza whole-virus vaccination // Vaccine. — 2005. — Vol. 23. — P. 1414–1425.
17. Halstead S. B., Rojanasuphot S., Sangkawibha N. Original antigenic sin in dengue // Am. J. Trop. Med. Hyg. — 1983 — Vol. 32, № 1. — P. 154–156.
18. Han J-F., Cao R Y., Deng Y.Q. et al. Antibody dependent enhancement infection of enterovirus 71 in vitro and in vivo // Virol J. — 2011. — Vol. 8 (10.1186/1743-422X-8-106).
19. Henchal E. A., McCown J. M., Burke D. S. et al. Epitopic analysis of antigenic determinants on the surface of dengue-2 virions using monoclonal antibodies // Am. J. Trop. Med. Hyg. — 1985. — Vol. 34. — P. 164–169.
20. Homsy J., Meyer M., Tateno M. et al. The Fc and not CD4 receptor mediates antibody enhancement of HIV infection in human cells // Science. —1989. — Vol. 16, № 244. — P. 1357–1360.
21. Iankov I. D., Pandey M., Harvey M. et al. Immunoglobulin G antibody-mediated enhancement of measles virus infection can bypass the protective antiviral immune response // J. Virol. — 2006. — Vol. 80, № 17. — P. 8530–8540.
22. Issel C J., Horohov D.W., Lea D.F. et al. Efficacy of inactivated whole-virus and subunit vaccines in preventing infection and disease caused by equine infectious anemia virus // J. Virol. — 1992. — Vol. 66. — P. 3398–3408.
23. Janjua N. Z., Skowronski D. M., Hottes T. S. et al. Seasonal influenza vaccine and increased risk of pandemic A/H1N1‐related illness: first detection of the association in British Columbia, Canada // Clin. Infect. Dis. — 2010. — Vol. 51, № 9. — Р. 1017–1027.
24. Jouanguy E., Lamhamedi-Cherradi S., Altare F. et al. Partial interferon-γ receptor 1 deficiency in a child with tuberculoid Bacillus Calmette-Guerin infection and a sibling with clinical tuberculosis // J. Clin. Invest. — 1997. — Vol. 100, № 11. — P. 2658–2664.
25. Kim J. H., Skountzou I., Compans R. et al. // Original antigenic sin responses to influenza viruses // J. Immunol. — 2009. — Vol. 183. — P. 3294–3301.
26. Klenerman P., Zinkernagel R. M. Original antigenic sin impairs cytotoxic T lymphocyte responses to viruses bearing variant epitopes // Nature. — 1998. —Vol. 394. — P. 482–485.
27. Kreil T. R., Eibl M. M. Pre- and postexposure protection by passive immunoglobulin but no enhancement of infection with a flavivirus in a mouse model // J. Viror. – 1997. — Vol. 71, № 4. — P. 2921–2927.
28. Marine W., Thomas J. Antigenic memory to influenza A viruses in man determined by monovalent vaccines // Postgraduate Medical J. 1979. Vol. 55. P. 98–108.
29. Robinson W. E, Montefiori D. C, Mitchell W. M . Antibody-dependent enhancement of human immunodeficiency virus type 1 infection // Lancet. —1988. — Vol. 9, № 1. — P. 790–794.
30. Rumyantsev S.N. The origin of individual differences in the course and severity of diseases // The Sci. World J. — 2006. — Vol. 6. — P. 1674–1704 (DOI 10.1100/tsw.2006.278).
31. Sasaki Y., Nomura A., Kusuhara K et al. Genetic basis of patients with Bacille Calmette-Guerin osteomyelitis in Japan: identification of dominant partial interferon-γ receptor 1 deficiency as a predominant type // J. Infect. Dis. — 2002. — Vol. 185. — P. 706–709.
32. Skowronski1 D. M., DeSerres G., Crowcroft N. et al. Association between the 2008–09 seasonal influenza vaccine and pandemic H1N1 illness during spring–summer 2009: four observational studies from Canada // PLoS Med. — 2010. — Vol. 7 — Is. 4 (e1000258. doi:10.1371/journal.pmed.1000258).
33. Takada A., Kawaoka Y. Antibody-dependent enhancement of viral infection: molecular mechanisms and in vivo implications // Rev Med Virol. — 2003. — Vol. 13, № 6. — P. 387–398.
34. Talbot E.A., Perkins M.D., Fagunes S. et al. Disseminated bacille Calmette-Guerin disease after vaccination: case report and review // Clin. Infect. Dis. — 1997. — Vol. 24, № 6. — P. 1139–1146.
35. Thomas H. I., Wilson S., O”Tolle C. M. et al. Differential maturation of avidity of IgG antibodies to gp41, p24 and p17 following infection with HIV-1 // Clin. Exp. Immunol. — 1996. — Vol. 103. — P. 185–191.
36. Thomas S., Redfern J. B., Lidbury B. et al. Antibody-dependent enhancement and vaccine development // Expert Rev. Vaccines. — 2006. — Vol. 5, № 4. — P. 409–412.
37. Tirado S. M., Yoon K. S. Antibody-dependent enchancement of virus infection and disease // Viral. Immunol. — 2003. — Vol. 164, № 1. — P. 69–86.
38. Wallace M. J., Smith D. W., Broom A. K. et al. Antibody-dependent enhancement of Murray Valley encephalitis virus virulence in mice // J. Gen. Virol. — 2003. — Vol. 84. — P. 1723–1728.
39. Wang S.Z., Rushlow K.E., Issel C.J. et al. Enhancement of EIAV replication and disease by immunization with a baculovirus-expressed recombinant envelope surface glycoprotein // Virol. — 1994. — Vol. 199. — P. 247–251.
40. Webster R. G. Original antigenic sin in ferrets: the response to sequential infections with influenza viruses // J. Immunology. — 1966. — Vol. 97. — P. 177–183.
41. Wrammert J., Smit K., Miller J. et al. Rapid cloning ofhigh-affinity human monoclonal antibodies against influenza virus // Nature. — 2008. — Vol. 453. — P. 667–671.
Библиографическое описание:
Супотницкий М.В . Неисследованные тупики вакцинации // Крымский журнал экспериментальной и клинической медицины. — 2011. — Т. 1, № 3–4. — С. 118–127.
Bibliographical description:
Supotnitskiy М.V. Unexplored deadlocks vaccination // Crimean Journal of experimental and clinical medicine. — 2011. — Vol. 1, № 3–4. — P. 118–127.
См. также:
Супотнiцький М.В . Чому ми не здолаемо ВIЛ/СНIД (Почему мы не победим ВИЧ/СПИД-пандемию) // I нфекц i йн i хворобию. — 2012. — № 1 (67). — С. 88–96; № 2 (68). — С. 104–114.
[1] Fc-рецепторы (Fc receptors) — представляют собой семейство молекул, каждый член которого распознает иммуноглобулин одного или нескольких родственных изотипов. Рецепторы этого типа входят в состав суперсемейства иммуноглобулинов. Fc-рецепторы для иммуноглобулинов присутствуют на поверхности мононуклеарных лейкоцитов, нейтрофилов, нормальных клеток-киллеров, эозинофилов, базофилов и тучных клеток. Взаимодействуя с Fc-областью иммуноглобулинов разных изотипов, эти рецепторы стимулируют, например, фагоцитоз, противоопухолевую цитотоксическую активность и дегрануляцию тучных клеток.

Михаил Васильевич Супотницкий
Российский микробиолог, полковник медицинской службы запаса, изобретатель, автор книг и статей по истории эпидемий чумы и других особо опасных инфекций, истории разработки и применения химического и биологического оружия. Заместитель главного редактора научно-практического журнала «Вестник войск РХБ защиты» Министерства обороны РФ.
Метки: 2011